第2节元素周期律和元素周期表第一课时元素周期律【配套课本】配山东版高中化学必修2第一章第二节【教学目标】知识与技能:1
使学生了解元素原子核外电子排布、原子半径、主要化合价的周期性变化,认识元素周期律
认识元素性质的周期性变化是元素原子核外电子排布周期性变化的结果,从而理解元素周期律的实质
掌握微粒半径变化规律
过程与方法:1
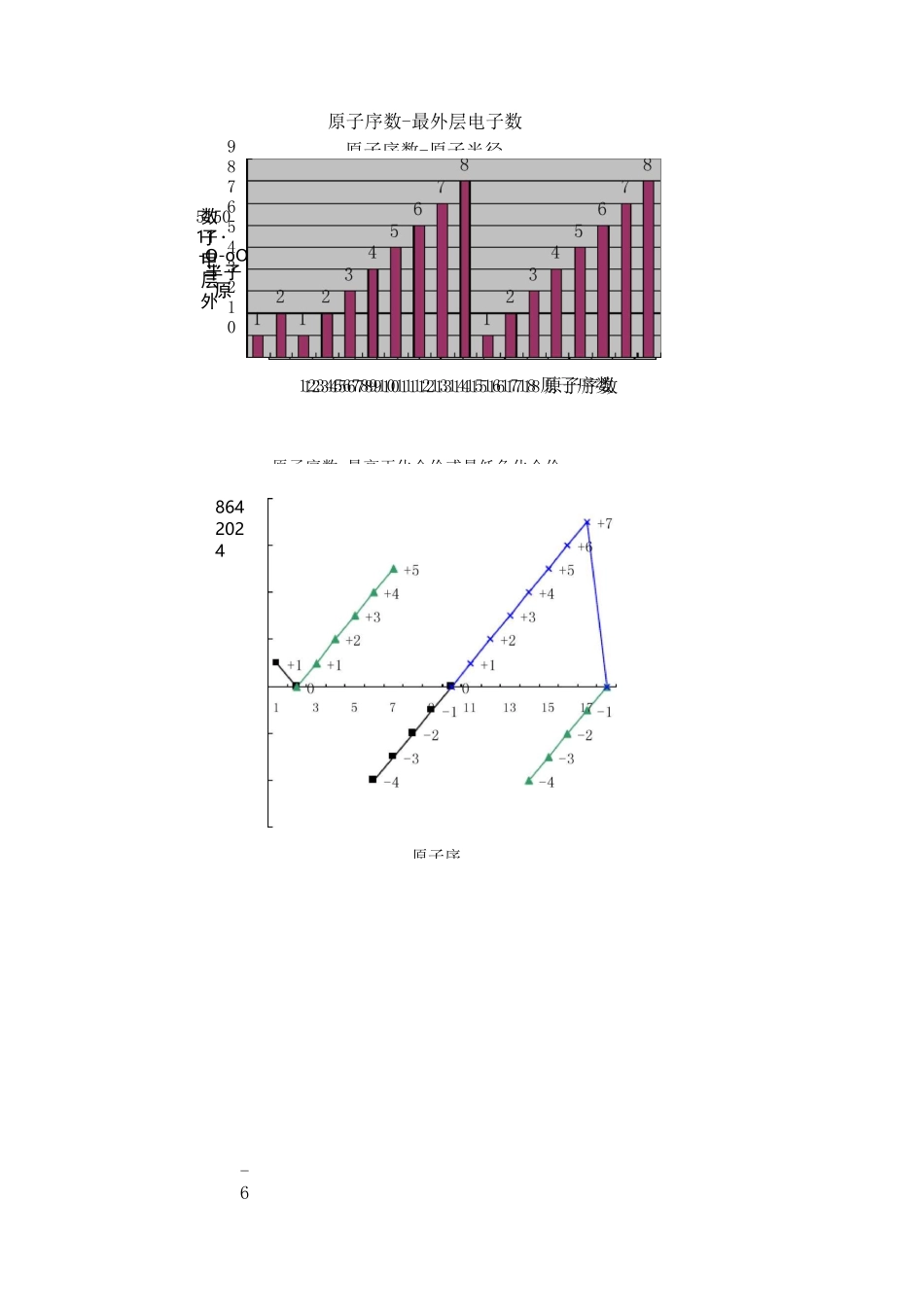
通过对元素周期律的初探,使学生会利用各种图表(直方图、折线图等)处理数据,提高他们分析、处理数据的能力
2•通过元素周期律的推出及其运用,初步培养学生分析问题、发现问题的能力;结合元素周期律的推出,使学生初步掌握从大量的事实和书籍中分析总结规律、透过现象看本质等可行抽象方法
【教学重点、难点】1
元素周期律的实质
微粒半径变化规律
【教学方法】归纳法、诱导探究法、练习法等
【教学过程】[引言]迄今为止,人类已经发现了一百多种元素,而各种元素的种类又是由该元素原子内的核电荷数即质子数决定的,那么,它们的结构与性质各有什么联系
这其中有没有什么规律
这就是我们本节课要研究的内容
[板书]第2节元素周期律和元素周期表一、元素周期律[讲述]下面,我们以核电荷数为1〜18的元素作为例子,从元素的核外电子排布、原子半径和主要化合价等方面来进行分析
[讲解]为了研究方便,我们把不同的元素按核电荷数由小到大的顺序对其进行编号,这种编号又叫原子序数
显然,原子序数在数值上是与这种原子的核电荷数相等的
原子序数是人为的,是人们强加给原子的,不是原子固有的
[板书]原子序数=核电荷数[师]下面,以小组为单位完成课本P]]“活动•探究”问题1表中所缺的数据
注意,核外电子排布包括电子层和各电子层上的电子数,不包括原子核和核内质子数
[学生活动]写出1〜18号元素的元素符号、原子结构示意图、电子层数和最外层电子数;组间交流
[师]阅读教材,了解怎样画直方图、怎样画