强电解质和弱电解质潮湿的手触摸正在工作的电器潮湿的手触摸正在工作的电器,,可能会发生触电事故可能会发生触电事故
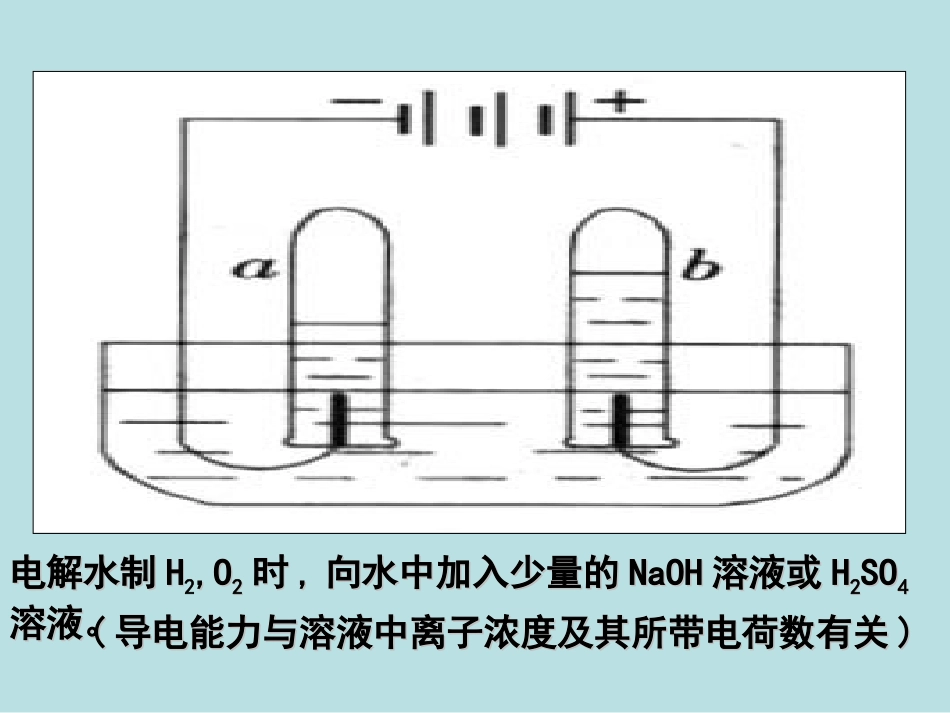
电解水制电解水制HH2,O,O22时时,,向水中加入少量的向水中加入少量的NaOHNaOH溶液或溶液或HH22SOSO44溶液
((导电能力与溶液中离子浓度及其所带电荷数有关导电能力与溶液中离子浓度及其所带电荷数有关))电解质:非电解质:(一)电解质和非电解质在水溶液中或熔融状态下能够导电的化合物
在水溶液中和熔融状态下都不能导电的化合物
思考题•SO2、NH3、Cl2的水溶液均能导电,它们是电解质吗
怎样区分电解质与非电解质
某些离子化合物(如Na2O、Na2O2、CaO)溶于水后电离出的离子并非其自身的,它们却属于电解质,为什么
电解质、非电解质的区分看水溶液或熔融状态下能否导电
(真正电离出自由移动的离子的物质才是电解质)①NaCl溶液②NaOH③H2SO4④Cu⑤CH3COOH⑥NH3·H2O⑦CO2⑧乙醇⑨H2O属于电解质的有:属于非电解质的有:②③⑤⑥⑨⑦⑧练一练:下列物质中1.醋酸和盐酸是常见的两种酸,根据你的经验,你认为它们的电离程度有无差异
你能设计实验验证你的猜想吗
电解质在水溶液中或熔化状态下离解成自由移动离子的过程实验1:测量物质的量浓度均为1mol/L盐酸、醋酸的pH
(资料:pH=-lgc(H+))pH试纸使用方法:1
将pH试纸放在表面皿上2
用洁净的玻璃棒沾取待测液点在试纸中央3
和标准比色卡对照物质的量浓度均为1mol/L的盐酸和醋酸与等质量镁条反应
实验2比较浓度均为1mol/L的盐酸和醋酸的导电性实验3盐酸和醋酸性质比较方法醋酸盐酸对实验现象的解释备注溶液的pH盐酸和醋酸都为等浓度的一元酸与镁条反应溶液的导电性大小慢快盐酸中氢离子浓度大盐酸中氢离子浓度大弱弱强强盐酸中离子浓度大盐酸中离子浓度大(二)强电解质和弱电解