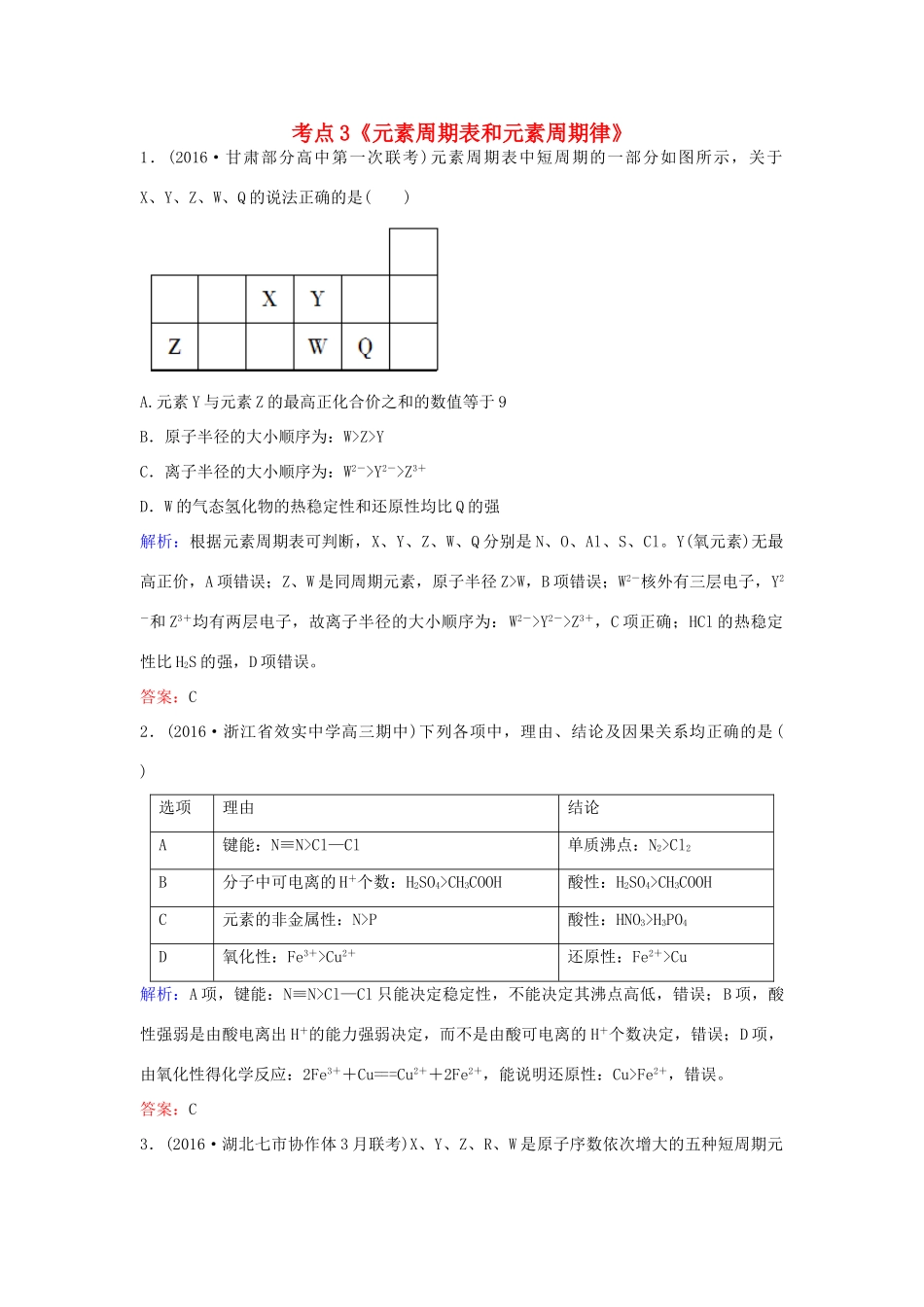
考点3《元素周期表和元素周期律》1.(2016·甘肃部分高中第一次联考)元素周期表中短周期的一部分如图所示,关于X、Y、Z、W、Q的说法正确的是()A
元素Y与元素Z的最高正化合价之和的数值等于9B.原子半径的大小顺序为:W>Z>YC.离子半径的大小顺序为:W2->Y2->Z3+D.W的气态氢化物的热稳定性和还原性均比Q的强解析:根据元素周期表可判断,X、Y、Z、W、Q分别是N、O、Al、S、Cl
Y(氧元素)无最高正价,A项错误;Z、W是同周期元素,原子半径Z>W,B项错误;W2-核外有三层电子,Y2-和Z3+均有两层电子,故离子半径的大小顺序为:W2->Y2->Z3+,C项正确;HCl的热稳定性比H2S的强,D项错误
答案:C2.(2016·浙江省效实中学高三期中)下列各项中,理由、结论及因果关系均正确的是()选项理由结论A键能:N≡N>Cl—Cl单质沸点:N2>Cl2B分子中可电离的H+个数:H2SO4>CH3COOH酸性:H2SO4>CH3COOHC元素的非金属性:N>P酸性:HNO3>H3PO4D氧化性:Fe3+>Cu2+还原性:Fe2+>Cu解析:A项,键能:N≡N>Cl—Cl只能决定稳定性,不能决定其沸点高低,错误;B项,酸性强弱是由酸电离出H+的能力强弱决定,而不是由酸可电离的H+个数决定,错误;D项,由氧化性得化学反应:2Fe3++Cu===Cu2++2Fe2+,能说明还原性:Cu>Fe2+,错误
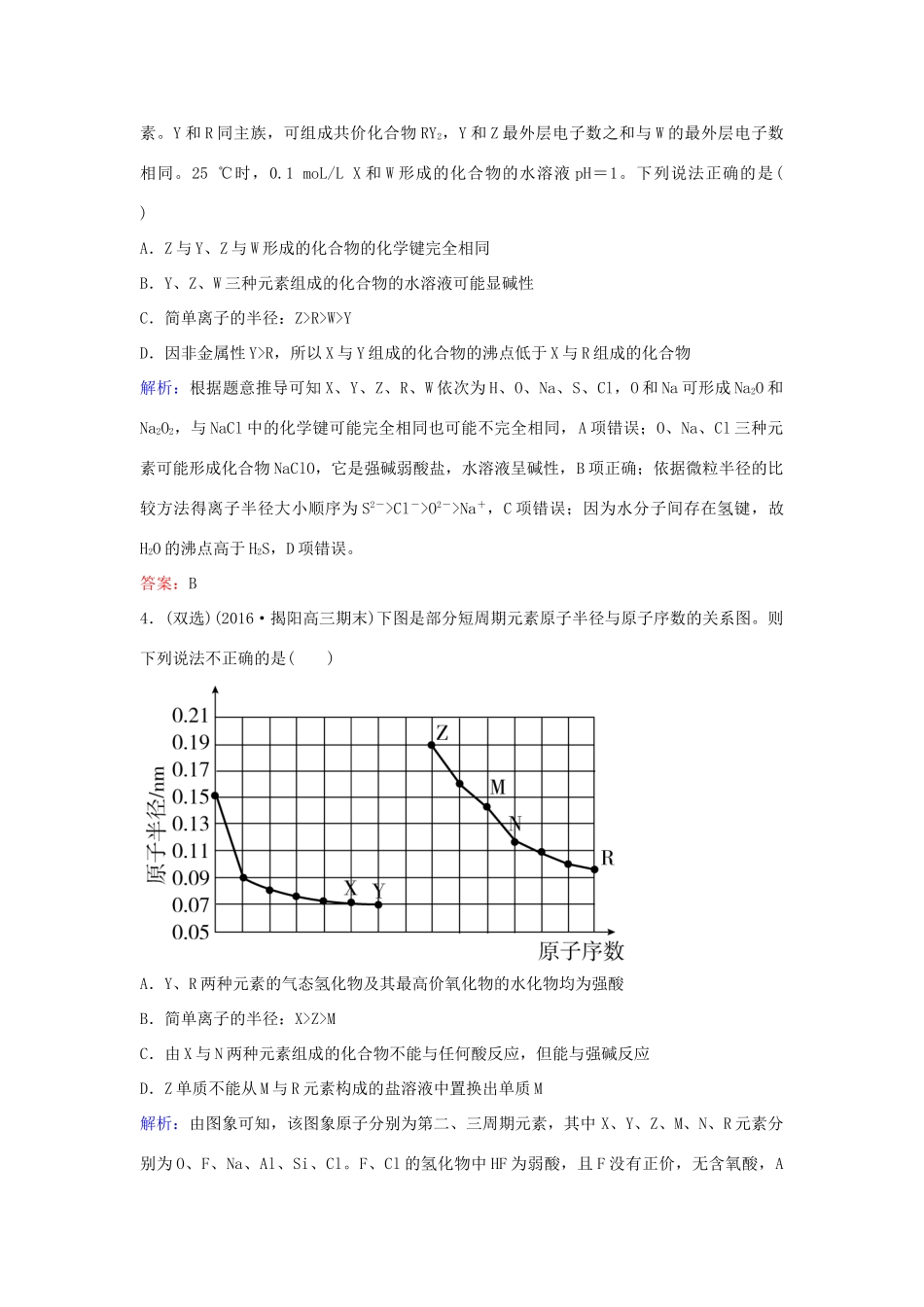
答案:C3.(2016·湖北七市协作体3月联考)X、Y、Z、R、W是原子序数依次增大的五种短周期元素
Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同
25℃时,0
1moL/LX和W形成的化合物的水溶液pH=1
下列说法正确的是()A.Z与Y、Z与W形成的化合物的化学键完全相同B.Y、Z、W三种元素组成的化合物的水溶液可能显碱