第一节氧化还原反应1
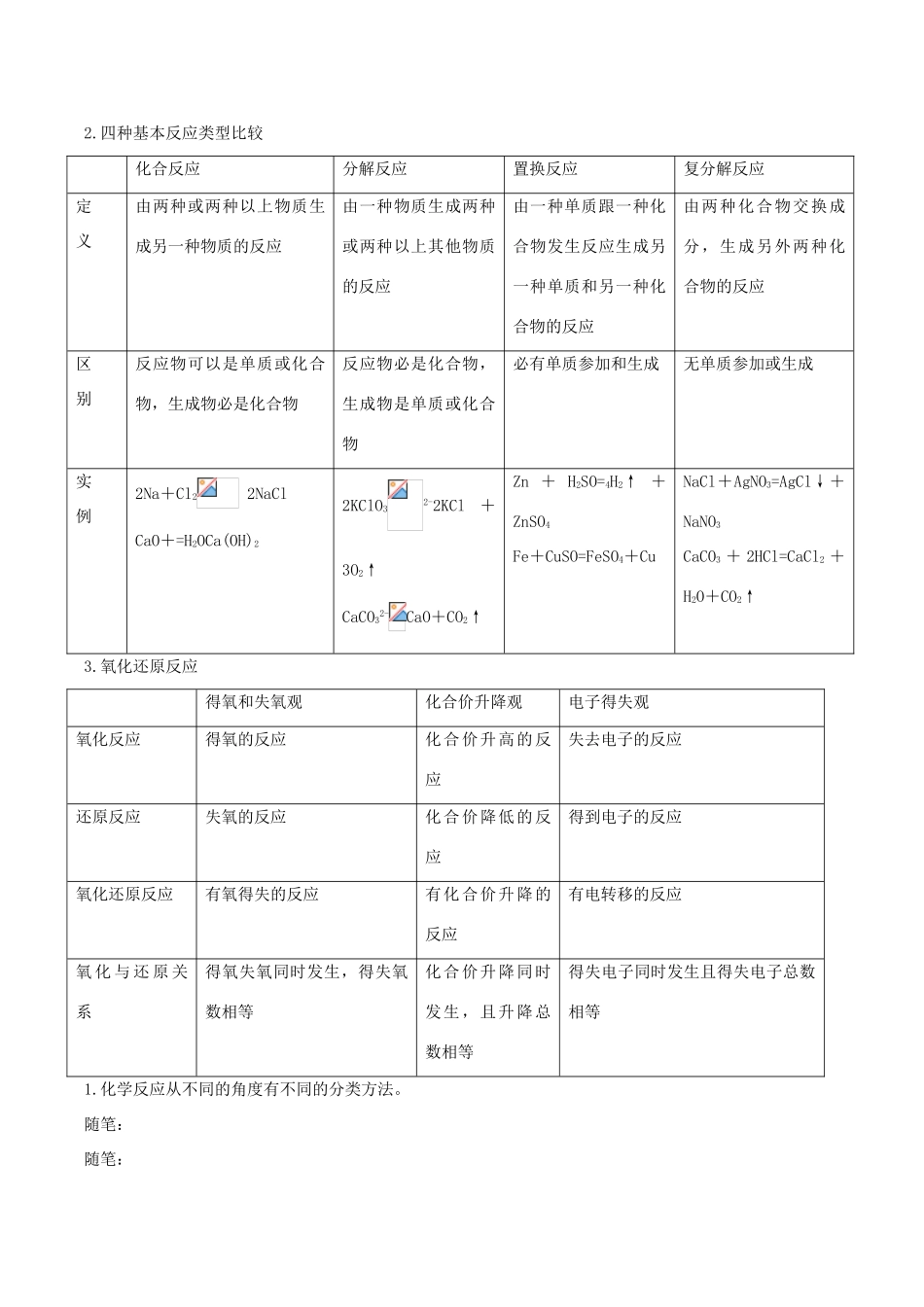
化学反应中的四种基本类型的反应(1)化合反应定义:由两种或两种以上的物质生成一种物质的反应,叫做化合反应
通式:A+B=AB如:2H2+O22H2OCaCO3+CO2+H2O=Ca(HCO3)2(2)分解反应定义:由一种物质生成两种或两种以上其他物质的反应,叫做分解反应
通式:AB=A+B如:2KClO32-2KCl+3O2↑NH4HCO32-NH3↑+H2O↑+CO2↑(3)置换反应定义:由一种单质跟一种化合物起反应,生成另一种单质和另一种化合物的反应,叫做置换反应
通式:A+BC=AC+B如:Fe+CuSO=FeSO4+CuC+2CuO2-2Cu+CO2↑(4)复分解反应定义:由两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应
通式:AB+CD=AD+CB如:Ba(OH)2+H2SO=BaSO4↓+2H2OBaCl2+Na2SO=BaSO4↓+2NaClMgCl2+2NaOH=Mg(OH)2↓+2NaClCaCO3+2HClCaCl2+H2CO3CO2↑+H2O2
氧化反应、还原反应反应名称得失氧的情况实例氧化名称物质得到氧的反应C+O2CO2,碳得到氧变成了CO2,碳发生的反应是氧化反应还原反应物质失去氧的反应CuO+H22-Cu+H2O,CuO失去氧变成了单质铜,氧化铜发生了还原反应课本知识导学运用课本知识诠解重要提示本节教材主要包括以下几部分内容1
化学反应的分类方法初中学习的化学反应的两种分类方法不能较深入地反应化学反应的本质,也不能包括所有的化学反应
化学反应从不同的角度有不同的分类方法
化学反应的常见分类方法:(1)依据反应前后物质种类的变化化合反应分解反应置换反应复分解反应(2)依据参加反应的微粒形式(3)依据反应中是否有电子转移(4)依据反应的能量转化方式化合反应分解反应置换反应复分解反应艾离子反应分子反应氧化还原反