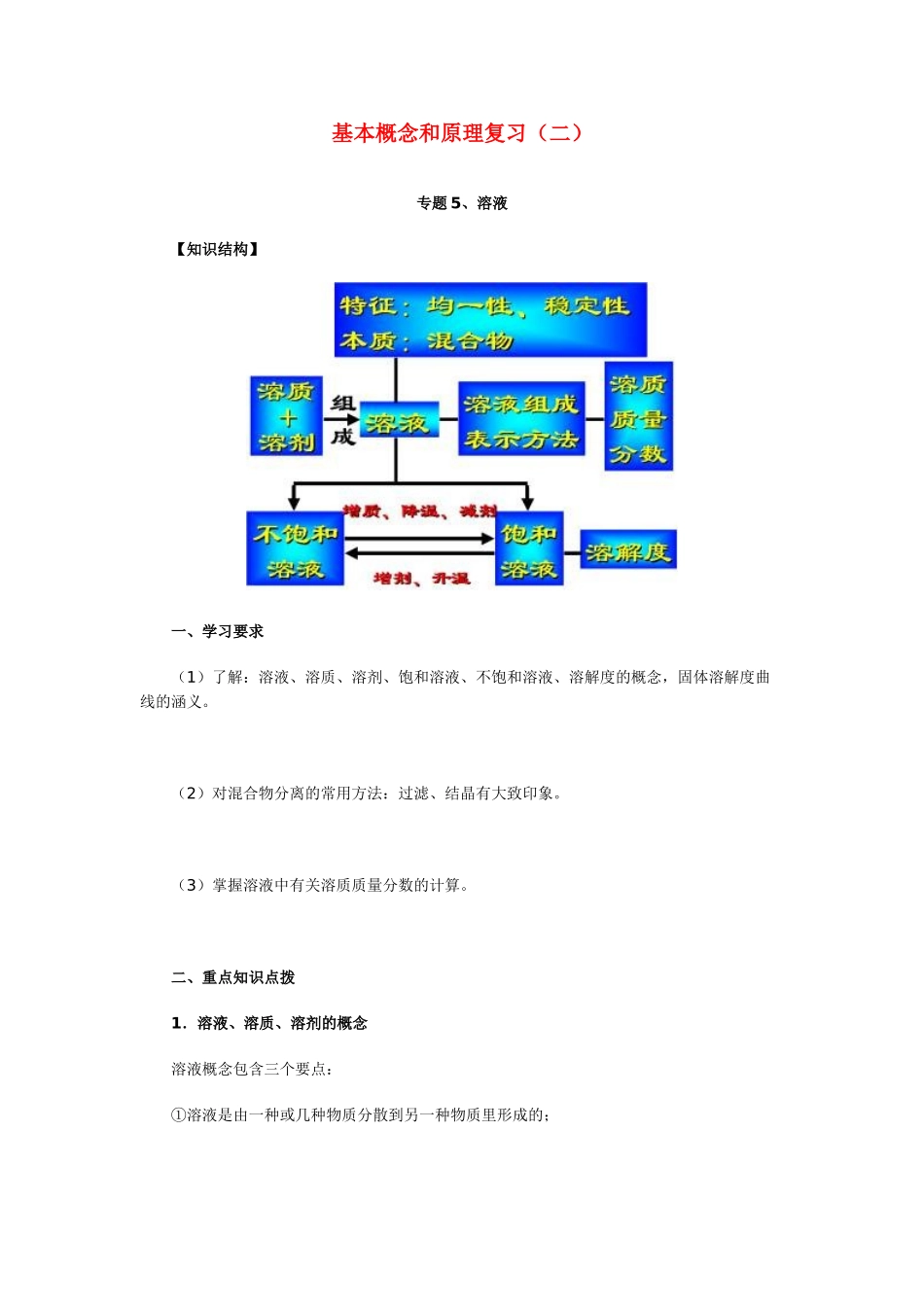
基本概念和原理复习(二)专题5、溶液【知识结构】一、学习要求(1)了解:溶液、溶质、溶剂、饱和溶液、不饱和溶液、溶解度的概念,固体溶解度曲线的涵义
(2)对混合物分离的常用方法:过滤、结晶有大致印象
(3)掌握溶液中有关溶质质量分数的计算
二、重点知识点拨1.溶液、溶质、溶剂的概念溶液概念包含三个要点:①溶液是由一种或几种物质分散到另一种物质里形成的;②其分散粒子为肉眼看不见的分子或离子,所以具有均一、稳定的特征;③溶液是混合物
应用:溶质、溶剂的判断:A、根据溶液的名称,一般溶质在前,溶剂在后
B、若物质在溶解时发生化学反应,在形成的溶液中,溶质是反应后分散到溶剂中的生成物
2.饱和溶液和不饱和溶液的判断及相互转化其转化关系如下:3.饱和溶液与浓溶液、不饱和溶液与稀溶液的关系饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液
一定温度下,对于同一溶质的饱和溶液要比不饱和溶液浓一些
4.溶解性与溶解度溶解性与溶解度是两个既有区别又有联系而且易于混淆的概念
溶解性是指一种物质溶解在另一种物质里的能力
溶解性的大小跟溶质和溶剂的性质有关,通常用易溶、微溶、可溶、难溶表示
溶解度是衡量某物质在某溶剂里溶解性大小的尺度,是溶解性定量的表示方法
5.溶解度曲线的涵义及其应用涵义:①表示物质在不同温度下的溶解度;②不同物质在同一温度下的溶解度;③物质的溶解度受温度影响的大小
应用:①判断某物质在不同温度下溶解度的大小;②比较同一温度下,不同物质溶解度的大小;③判断不同物质溶解度受温度影响的变化趋势;④确定混合物分离、提纯的方法
6.混合物分离的两种方法——过滤和结晶过滤是分离不溶于液体的固体和液体的方法,结晶是分离几种可溶性固体的方法
7.溶液组成的表示方法溶液组成用溶质的质量占全部溶液质量的分数来表示:★溶解度与溶质质量分数的区别:溶解度和溶质的质量分数项目溶解度溶质的质量分数量的关