第一章从实验学化学第二节化学计量在实验中的应用第2课时摩尔质量【复习回顾】物质的量、阿伏伽德罗常数1、定义:表示含有一定数目粒子的集体的物理量3、单位:摩尔,简称摩,符号是mol2、符号为n4、使用物质的量注意事项:①物质的量是一个专用名词,不能拆开
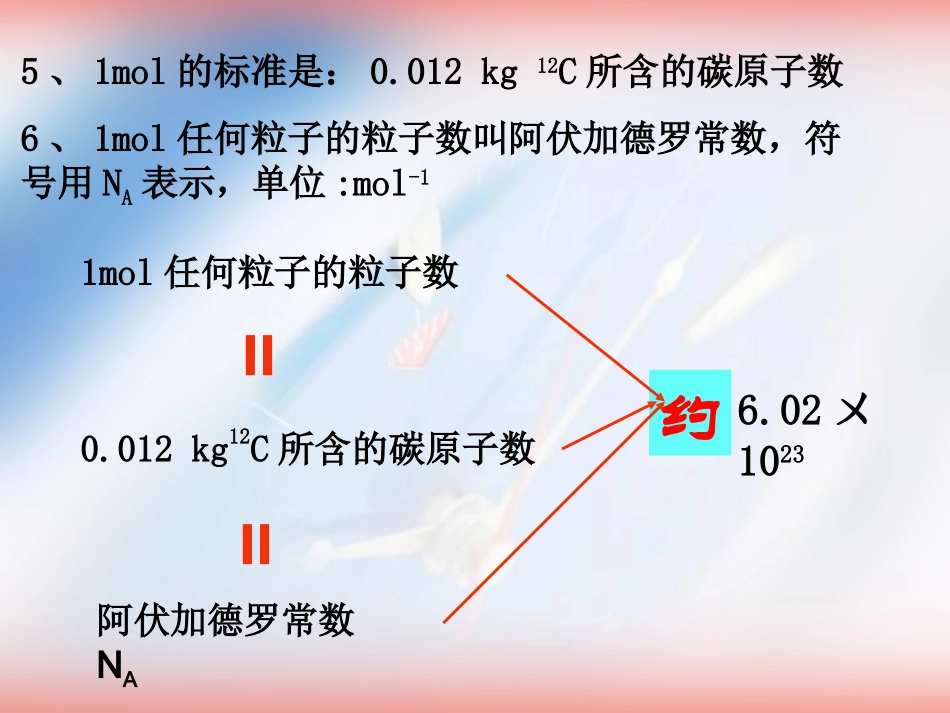
②使用mol作单位,应用符号或化学式指明粒子的种类5、1mol的标准是:0
012kg12C所含的碳原子数6、1mol任何粒子的粒子数叫阿伏加德罗常数,符号用NA表示,单位:mol-11mol任何粒子的粒子数=0
012kg12C所含的碳原子数=阿伏加德罗常数NA6
02ㄨ1023约ANN7、n、N、NA的关系:8、推论:2121NNnn(粒子物质的量之比=粒子个数比)1.下列说法中,不正确的是()A.1mol任何物质都含有6
02×1023个原子B.0
012kg12C约含有6
02×1023个碳原子C.阿伏加德罗常数表示的粒子“集体”就是1molD.使用摩尔这一单位时必须指明粒子的名称A【复习练习】2.amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为_________a4bmol-1【问题延伸】1mol物质的质量到底有多大
粒子符号物质的式量每个粒子的质量(g/个)1摩物质含有的粒子数(个)1摩物质质量(g)C121
993X10-23Fe569
032X10-23H2SO4981
628X10-22H2O182
990X10-23Na+233
821X10-23OH-172
824X10-23NANANANANANA125698182317结论:1mol任何微粒或物质的质量以克为单位时,在数值上等于该微粒的相对原子质量或相对分子质量
【归纳整理】摩尔质量1
定义:单位物质的量(1mol)的物质的质量2
单位:g/mol4
数值:以克每摩尔为单位时,摩尔质量在数值上等于该微粒的相对原子质量或相对