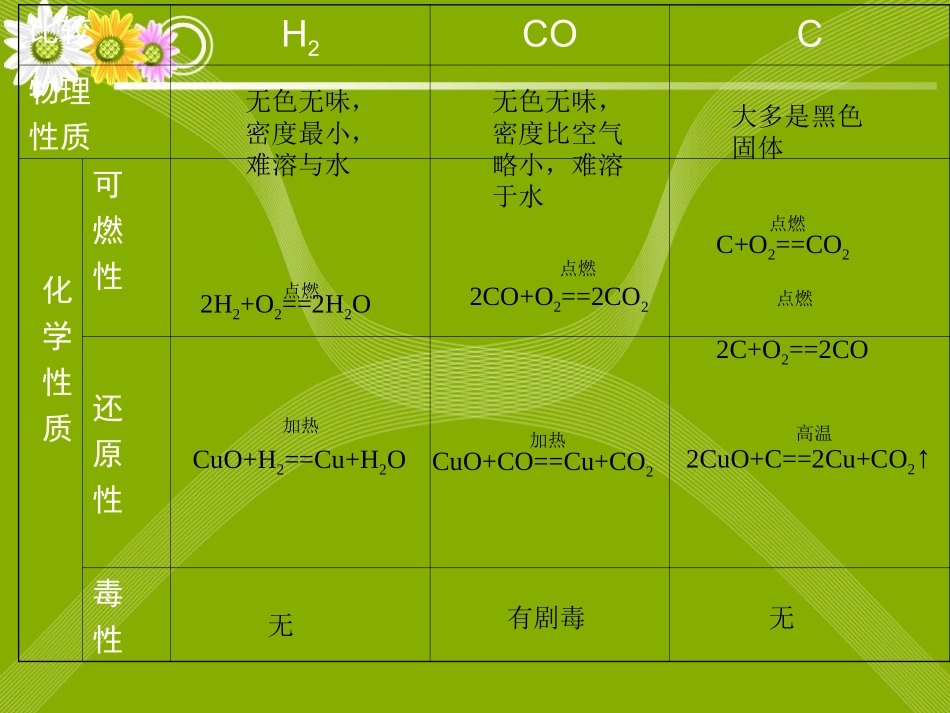
氢气、木炭、一氧化碳还原氧化铜氢气、木炭、一氧化碳还原氧化铜的比较的比较比较H2COC物理性质化学性质可燃性还原性毒性无色无味,密度最小,难溶与水无色无味,密度比空气略小,难溶于水大多是黑色固体无有剧毒无2H2+O2==2H2O点燃2CO+O2==2CO2点燃C+O2==CO22C+O2==2CO点燃点燃CuO+H2==Cu+H2O加热CuO+CO==Cu+CO2加热2CuO+C==2Cu+CO2↑高温CO+CuO===Cu+CO2加热C+2CuO===2Cu+CO2↑高温CuO+H2==Cu+H2O加热一、碳跟氧化铜的反应C+CuO澄清石灰水让我们来思考这个反应的现象1、试管内有红色物质生成2、澄清石灰水变浑浊C+2CuO===CO2↑+2Cu高温二、氢气跟氧化铜的反应1:装置2
实验操作:•1
装入药品•2
安装装置•3
通氢气排出空气•4
反应完全后停止加热•6
试管冷却后停止通氢气先检验H2的纯度
实验注意事项:•1
通氢气前要先检验纯度•2
安装时,试管口要略向下倾斜(防止生成的水倒流回试管底部使其炸裂)•3
通氢气的导管要插到试管底部且靠上层(一方面将试管里的空气排尽,一方面保证氢气与氧化铜充分接触
实验时,要先通氢气排空气,后加热•5
结束时,要先熄灯,待试管冷却后在停止通氢气
(防止生成的铜又被导管中的空气氧化成氧化铜
现象:氧化铜由黑色转变为红色光亮物质,同时管口有水滴生成
化学方程式CuO+H2——Cu+H2O失去氧,发生还原反应,有氧化性得到氧,发生氧化反应,有还原性氢气在加热的条件下能还原金属氧化物生成相应的金属单质和水
•H2+WO3——•H2+Fe2O3——高温高温W+3H2O2Fe+3H2O332
指出下列装置中的错误,并思考这样做可能产生的后果
试管口没有略向下倾斜通氢导管没有插到试管底部试管加了橡皮塞思考:•氢气