第2课时元素周期律学习目标核心素养建构1
通过分析1~18号元素原子核外电子排布、原子半径、主要化合价的变化,总结出它们的递变规律,并由此认识元素周期律
初步认识元素性质的周期性变化是元素原子核外电子排布周期性变化的必然结果
[知识梳理]一、原子结构的周期性变化1
原子序数(1)概念:按核电荷数由小到大的顺序给元素编号,这种编号叫做原子序数
(2)数量关系:原子序数=质子数=核外电子数=核电荷数
原子结构变化规律(1)原子最外层电子排布的规律性变化观察上图回答问题:从3~18号元素随着原子序数的递增,最外电子层上的电子数重复出现从1递增到8的变化,说明元素原子的最外层电子排布呈现周期性变化
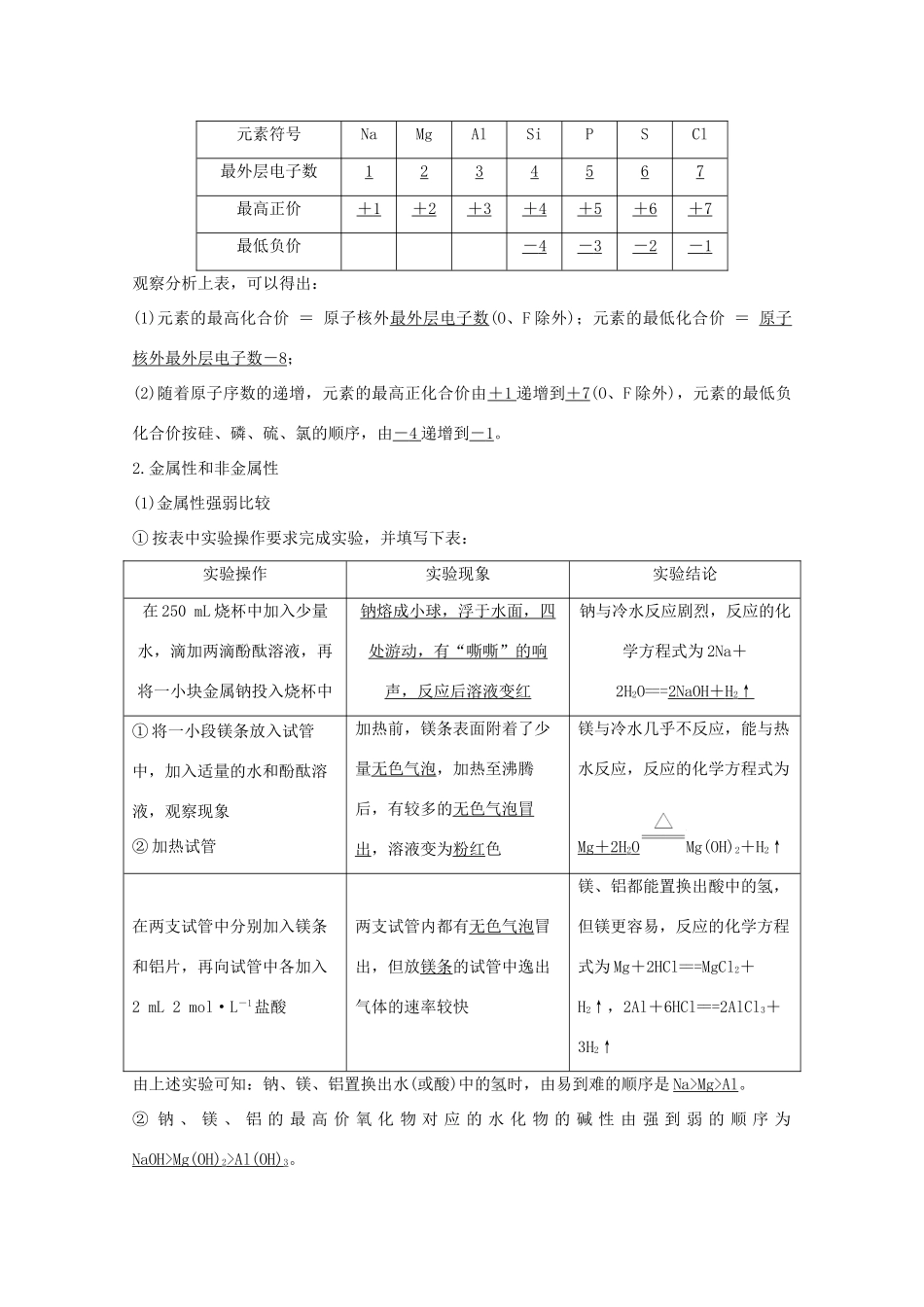
(2)元素原子半径的变化规律下表为原子序数为3~9和11~17元素的原子半径:3~9号3Li(锂)4Be(铍)5B(硼)6C(碳)7N(氮)8O(氧)9F(氟)元素原子半径/pm152111887770666411~17号元素11Na(钠)12Mg(镁)13Al(铝)14Si(硅)15P(磷)16S(硫)17Cl(氯)原子半径/pm18616014311711010499注:1pm=10-12m从上表可以得到:随着原子序数的递增,元素原子半径(稀有气体除外)呈现周期性变化
3~9号元素、11~17号元素原子半径随着核电荷数的递增都逐渐减小
【自主思考】1
“1~18号元素的原子半径随着核电荷数的递增逐渐减小”这句话是否正确
①3~9号元素,11~17号元素的原子半径随着核电荷数的递增逐渐减小,变化规律是周期性的,而不是一直减小;②2、10、18号等稀有气体元素的原子半径与其他元素的原子半径测定标准不同,不具有可比性
③核电荷数小的元素其原子半径不一定小,如Li>Cl
解释下列问题:(1)对于电子层数相同的原子,为什么其核电荷数越多,原子半径越小(稀有气体除