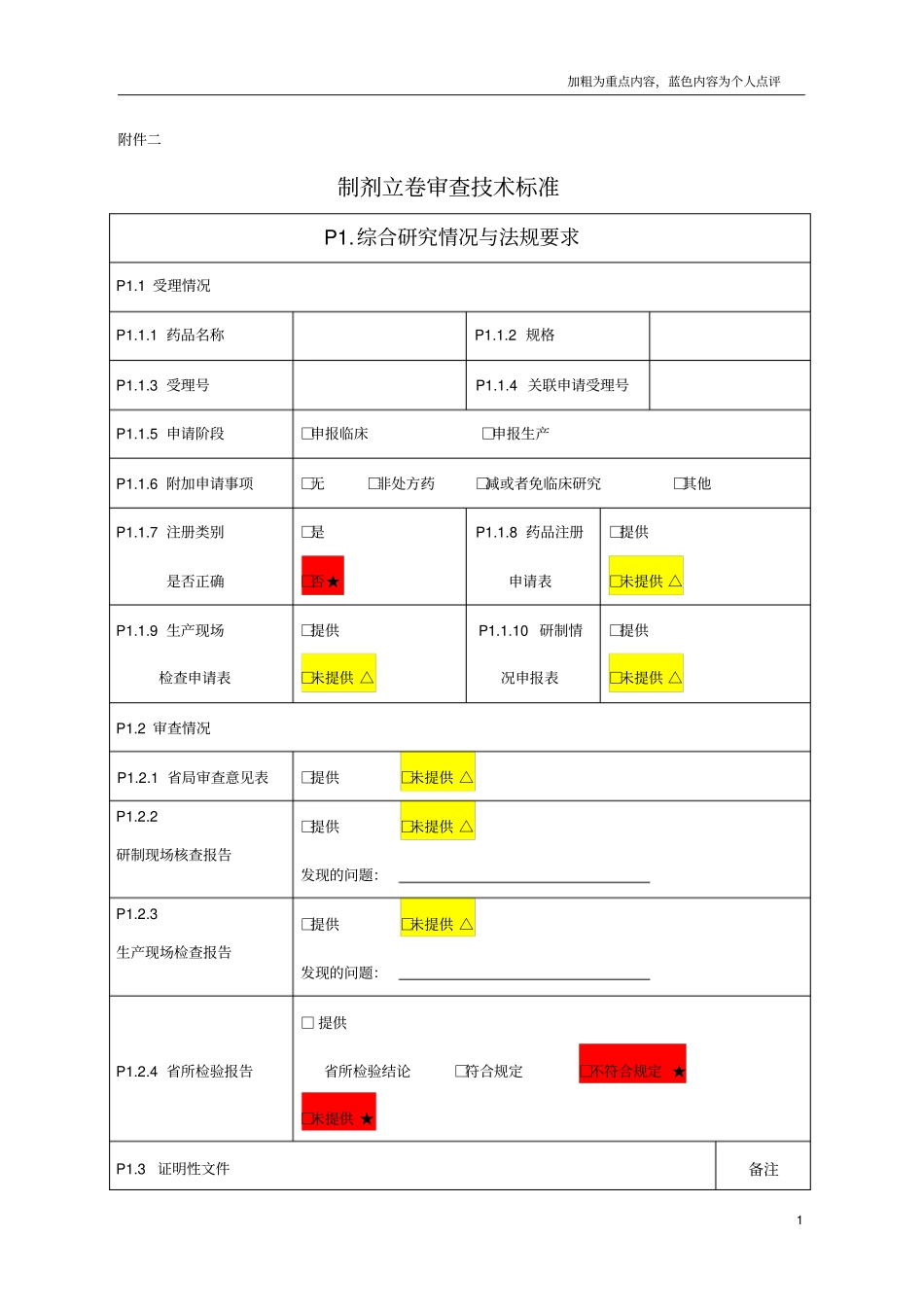
加粗为重点内容,蓝色内容为个人点评1 附件二制剂立卷审查技术标准P1
综合研究情况与法规要求P1
1 受理情况P1
1 药品名称P1
2 规格P1
3 受理号P1
4 关联申请受理号P1
5 申请阶段□申报临床□申报生产P1
6 附加申请事项□无□非处方药□减或者免临床研究□其他P1
7 注册类别是否正确□是□否★P1
8 药品注册申请表□提供□未提供 △P1
9 生产现场检查申请表□提供□未提供 △P1
10 研制情况申报表□提供□未提供 △P1
2 审查情况P1
1 省局审查意见表□提供□未提供 △P1
2 研制现场核查报告□提供□未提供 △发现的问题:P1
3 生产现场检查报告□提供□未提供 △发现的问题:P1
4 省所检验报告□ 提供省所检验结论□符合规定□不符合规定 ★□未提供 ★P1
3 证明性文件备注加粗为重点内容,蓝色内容为个人点评2 P1
1 《企业法人营业执照》□提供□未提供 △P1
2 《药品生产许可证》范围是否包含本剂型□是□否△P1
3 相关剂型 《药品生产质量管理规范》认证证书□提供□未提供□有说明□无说明 △□不适用P1
4 《药物临床试验批件》□提供□未提供 △□不适用P1
4 专利情况P1
1 药物在中国的专利及权属状态的说明以及对他人的专利不构成侵权的声明□提供□未提供 △P1
5 特殊管理药品麻醉药品、精神药品、医疗用毒性药品及放射性药品研制立项批复文件□提供□未提供 △□不适用 (非特药 )P1
6 原研药物基本情况□提供上市国家□上市 / □国内首次进口时间生产企业名称□未提供 △P1
7 原料药加粗为重点内容,蓝色内容为个人点评3 P1
1 □国产原料药是否提供了所有原料药的下列资料:P1
1批准证明文件或受理通知书P1
2药品质量标准