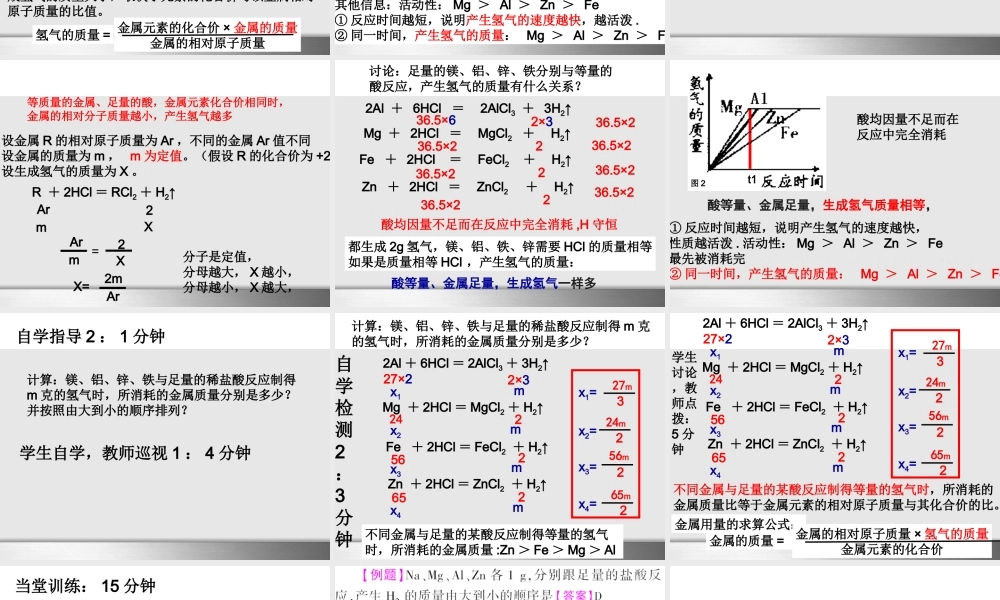
金属的化学性质 图像专题第八单元 金属和金属材料李小球2011.12.2学习目标: 1 分钟1. 掌握等质量的不同金属与足量的酸反应的规律2. 掌握足量金属与等量的酸反应的规律3. 掌握不同金属与足量的酸反应的规律 计算:(相同质量) m 克镁、铝、锌、铁,分别与足量的稀盐酸反应,产生氢气的质量分别是多少? 并按照由大到小的顺序排列?(相对原子质量 镁: 24 铝: 27 铁: 56 锌:65 )学生自学,教师巡视 1 : 4 分钟自学指导 1 : 1 分钟计算:(相同质量) m 克镁、铝、锌、铁,分别与足量的稀盐酸反应,产生氢气的质量分别是多少并排序?等质量的不同金属与足量的酸反应产生氢气的质量:Al > Mg > Fe > Zn Mg + 2HCl = MgCl2 + H2↑2Al + 6HCl = 2AlCl3 + 3H2↑Zn + 2HCl = ZnCl2 + H2↑Fe + 2HCl = FeCl2 + H2↑2422256652×327×2 mmmm2m242m562m656m27×23m27x1x2x3x4x1=x2=x3=x4=自学检测 1 : 3 分钟 Mg + 2HCl = MgCl2 + H2↑2Al + 6HCl = 2AlCl3 + 3H2↑Zn + 2HCl = ZnCl2 + H2↑Fe + 2HCl = FeCl2 + H2↑2422256652×327×2 mmmm2m242m562m656m27×23m27x1x2x3x4x1=x2=x3=x4=等质量的不同金属与足量酸(盐酸或稀硫酸)反应,生成氢气的质量大小,取决于元素的化合价与该金属相对原子质量的比值。金属元素的化合价 × 金属的质量金属的相对原子质量氢气的质量 =学生讨论,教师点拨:5 分钟图 1t1 t2 t3t4●●●●其他信息:活动性: Mg > Al > Zn > Fe① 反应时间越短,说明产生氢气的速度越快,越活泼 .② 同一时间,产生氢气的质量: Mg > Al > Zn > Fe等质量的不同金属酸足量等质量的不同金属与足量的酸反应产生氢气的质量:Al > Mg > Fe > Zn金属元素的化合价 × 金属的质量金属的相对原子质量氢气的质量 =讨论:等质量的金属、足量的酸,当金属元素化合价相同时,有什么规律?等质量的金属、足量的酸,金属元素化合价相同时,金属的相对分子质量越小,产生氢气越多 R + 2HCl = RCl2 + H2↑设金属 R 的相对原子质量为 Ar ,不同的金属 Ar 值不同设金属的质量为 m , m 为定值。(假设 R 的化合价为 +2 )设生成氢气的质量为 X 。Ar2mXAr2mX=X=2mAr分子是定值,分母越大, X 越小,分母越小, X 越大,讨论:足量的镁、铝、锌、铁...