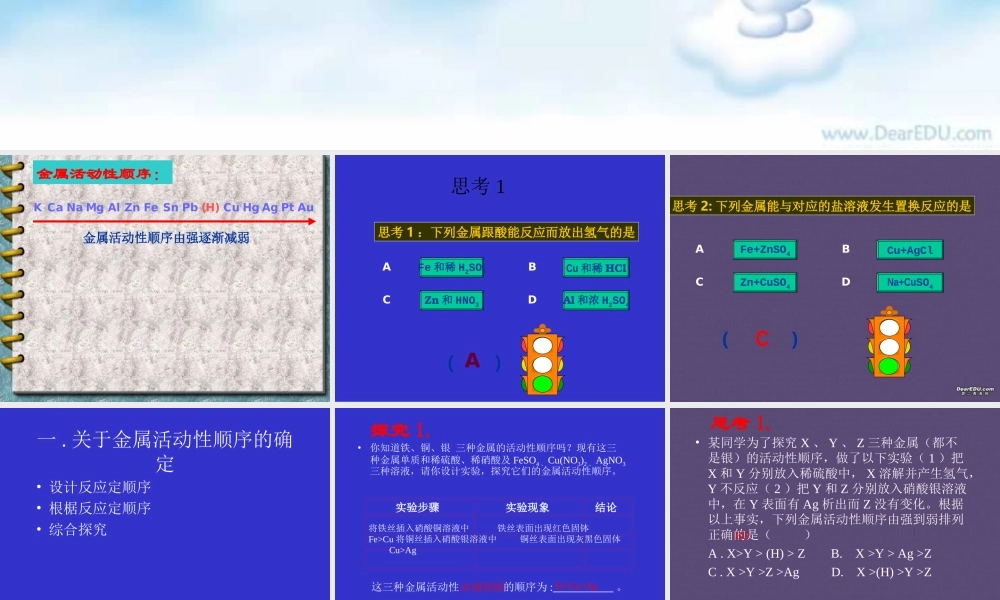
专题复习 金属活动性顺序与置换反应金属活动性K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性顺序由强逐渐减弱金属活动性顺序: Fe 和稀 H2SO4思考 1 :下列金属跟酸能反应而放出氢气的是ABCDCu 和稀 HClZn 和 HNO3Al 和浓 H2SO4( )A思考 1Fe+ZnSO4思考 2: 下列金属能与对应的盐溶液发生置换反应的是ABCDCu+AgClZn+CuSO4Na+CuSO4( )C 一
关于金属活动性顺序的确定• 设计反应定顺序• 根椐反应定顺序• 综合探究 探究 1
•你知道铁、铜、银 三种金属的活动性顺序吗
现有这三种金属单质和稀硫酸、稀硝酸及 FeSO4 、Cu(NO3)2 、AgNO3三种溶液,请你设计实验,探究它们的金属活动性顺序
实验步骤 实验现象 结论 这三种金属活动性由强到弱的顺序为 :
将铁丝插入硝酸铜溶液中 铁丝表面出现红色固钵 Fe>Cu 将铜丝插入硝酸银溶液中 铜丝表面出现灰黑色固体 Cu>AgFe>Cu>Ag思考 1
• 某同学为了探究 X 、 Y 、 Z 三种金属(都不是银)的活动性顺序,做了以下实验( 1 )把X 和 Y 分别放入稀硫酸中, X 溶解并产生氢气,Y 不反应( 2 )把 Y 和 Z 分别放入硝酸银溶液中,在 Y 表面有 Ag 析出而 Z 没有变化
根据以上事实,下列金属活动性顺序由强到弱排列正确的是( ) A
X>Y > (H) > Z B
X >Y > Ag >Z C
X >Y >Z >Ag D
X >(H) >Y >ZBD 思考 2
•置换反应是化学反应的基本类型之一:( 1 )金属与盐溶液之间的置换反应,通常是活动性较强的金属可把活动性较弱的金属从它的盐溶液中置换出来
如铜与硝酸银溶液发生的反应,反应的化学方程式为
( 2 )非金属单质