医疗器械产品放行程序文件编号:1 目的使产品质量控制的各环节进一步细化,确保出厂产品安全有效
2 适用范围本程序包括原材料放行、生产过程产品放行、成品检验放行及成品放行
3 职责与权限3
1 主管技术质量的分管领导担任总质量授权人;3
2 原材料检验人担任原材料质量授权人;3
3 过程控制负责人担任生产过程质量授权人;3
4 质量管理部负责人担任产品检验质量授权人;3
5 总质量授权人担任成品放行质量授权人;3
6 总质量授权人可决定增设部门二级质量授权人,提名部门主要负责人或另设专人,报公司批准受权后生效
4 产品放行控制程序4
1 原材料质量放行程序:4
1 采购部门将采购原材料送质检部检验
原材料质量授权人在对原材料实施放行时,应审核下列过程是否符合要求,若其中一项不合格则不予放行:a)采购过程是否符合《采购控制程序》;b)原材料的供方是否发生变化,是否在合格供方目录内;c)原材料的材料组成是否发生变化;d)原材料是否具有进货检验报告;e)进货检验过程是否满足《采购产品验证控制程序》及检验操作规程;f)检验设备是否在检定周期内;g)检验人员是否经培训上岗;h)检验环境是否符合要求
以上符合要求后原材料质量授权人在《原材料放行证书》 签字放行, 采购的原材料不合格按不合格品控制程序执行
2 原材料质量放行流程图4
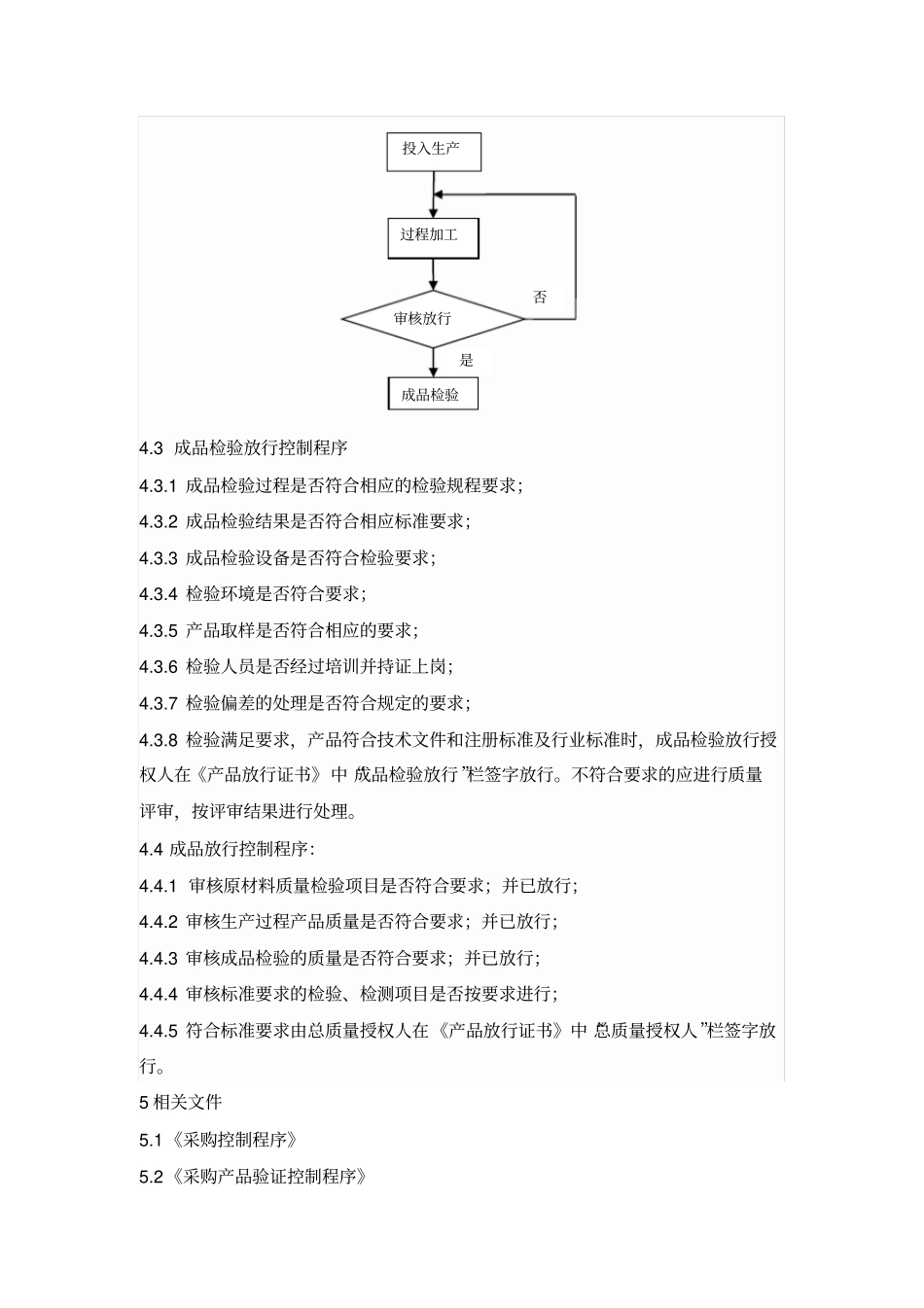
2 生产过程产品质量放行控制程序:4
1 生产过程质量授权人根据相应的生产工艺文件及管理要求全面对生产过程进行监控,监控的内容包括原材料状态、设备状态、生产环境状态、工艺参数及生产人员的培训;4
2 生产过程质量授权人对产品的特殊工序与关键工序进行审核;4
3 生产过程质量授权人根据相应的过程质量要求组织过程产品的质量检验、产品材料及零组件抽检,只有过程产品质量符合规定的要求才可以转入下一工序;4
4 生产过程质量授权人对生产记录、