审评四部增加规格品种的处理原则6 月 25 日经部长协调会再次讨论,确定了增加规格品种的基本处理原则和思路,根据会议讨论认为,原则上按照2004 年 1 月 4 日“关于规范增加规格品种审评部间协调会会议纪要”的内容进行品种处理
由于增加规格情况的复杂性和多样性,另外再强调以下几点:1、对于已批上市规格,除可能存在安全性隐患问题的规格外,如 20mg 及以上规格的七叶皂苷钠,其他情况下的申请一般给予批准;2、对于装量符合倍数关系的粉针剂,还应结合成人用药的起始剂量考虑,即为成人单次剂量的倍数同时又在成人用法用量范围内,否则将不予批准
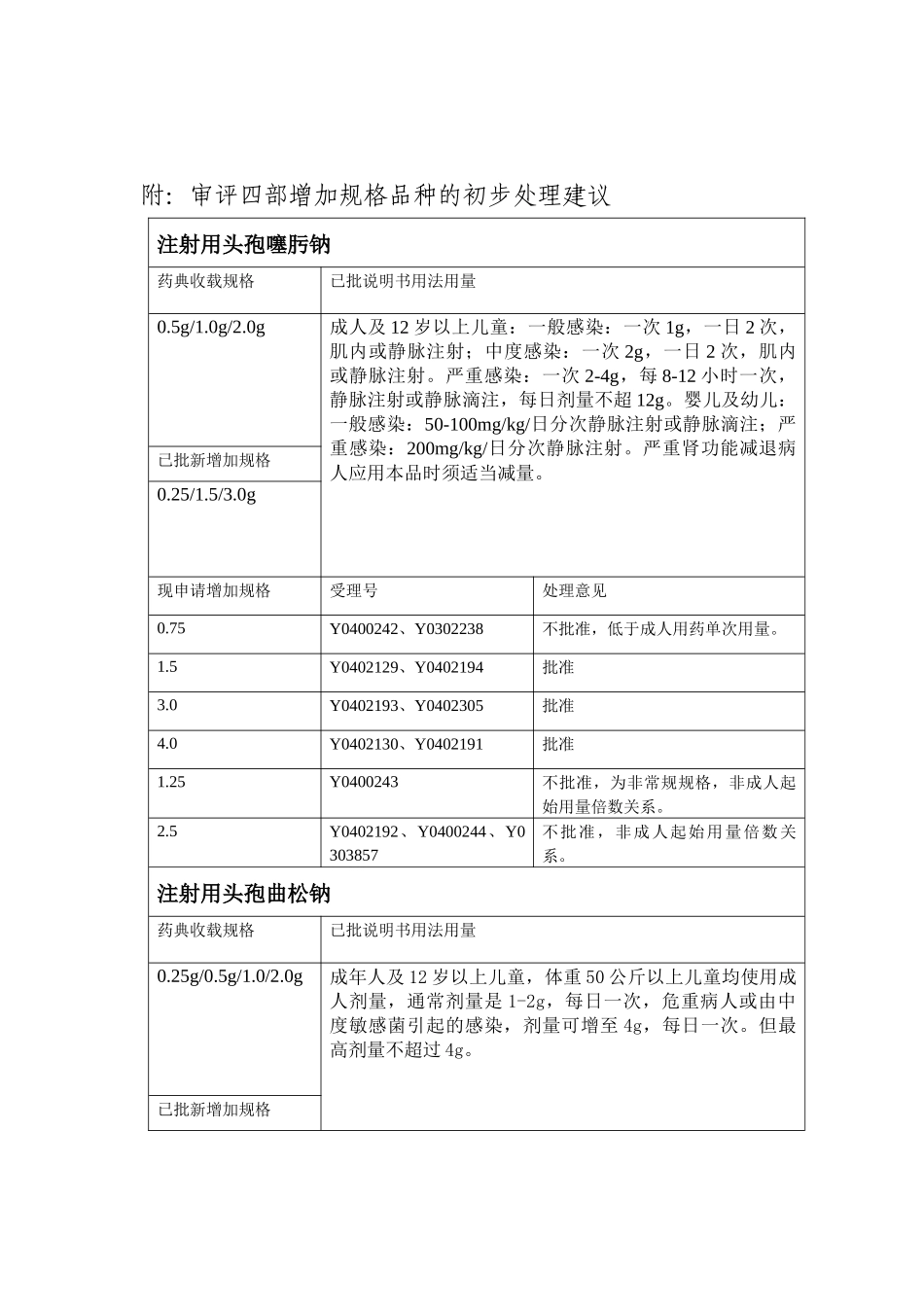
如注射用头孢噻肟钠,申请 2
5g,该规格在已批用量范围内,且为最低规格(0
5g)整数倍,但非成人起始剂量(1g)整数倍,因此不予批准;3、对于申请增加儿童规格的或者说低于成人单次最低剂量规格的,由于根据说明书中儿童用法用量按公斤体重计算将可能派生出多种规格,因此原则上不同意增加儿童规格,已上市的低于成人单次最低剂量的规格可视为儿童规格; 也即相当于执行纪要内容“对于低于成人单次最低剂量的规格不予批准
”4、对于说明书中有“严重感染增加至…g”的,应视该规格为特定规格,而不是从一般感染到严重感染之间的剂量范围内的多种规格;如注射用头孢曲松钠,通常剂量是 1~2 g,每日一次,严重感染或危重病人,剂量可增至 4 g,此时可以增加的对于严重感染的规格为 4 g,而不是 2~4 g
5、对于小水针、大输液增加规格品种,除以上条款外,需特别注意应同时考虑容积、浓度及主药量三方面因素,同时符合上述三方面条件,即主药含量在单次用量范围内,容积为常规装量,浓度与已上市规格相同,否则一般不予批准
对于增加规格品种,不批准的结论统一如下:(1)对于规格大于单次用量最大剂量的规格,结论为:根据本品说明书中用法用量“……”,所申请增加的规格大于本品临床单次应用的