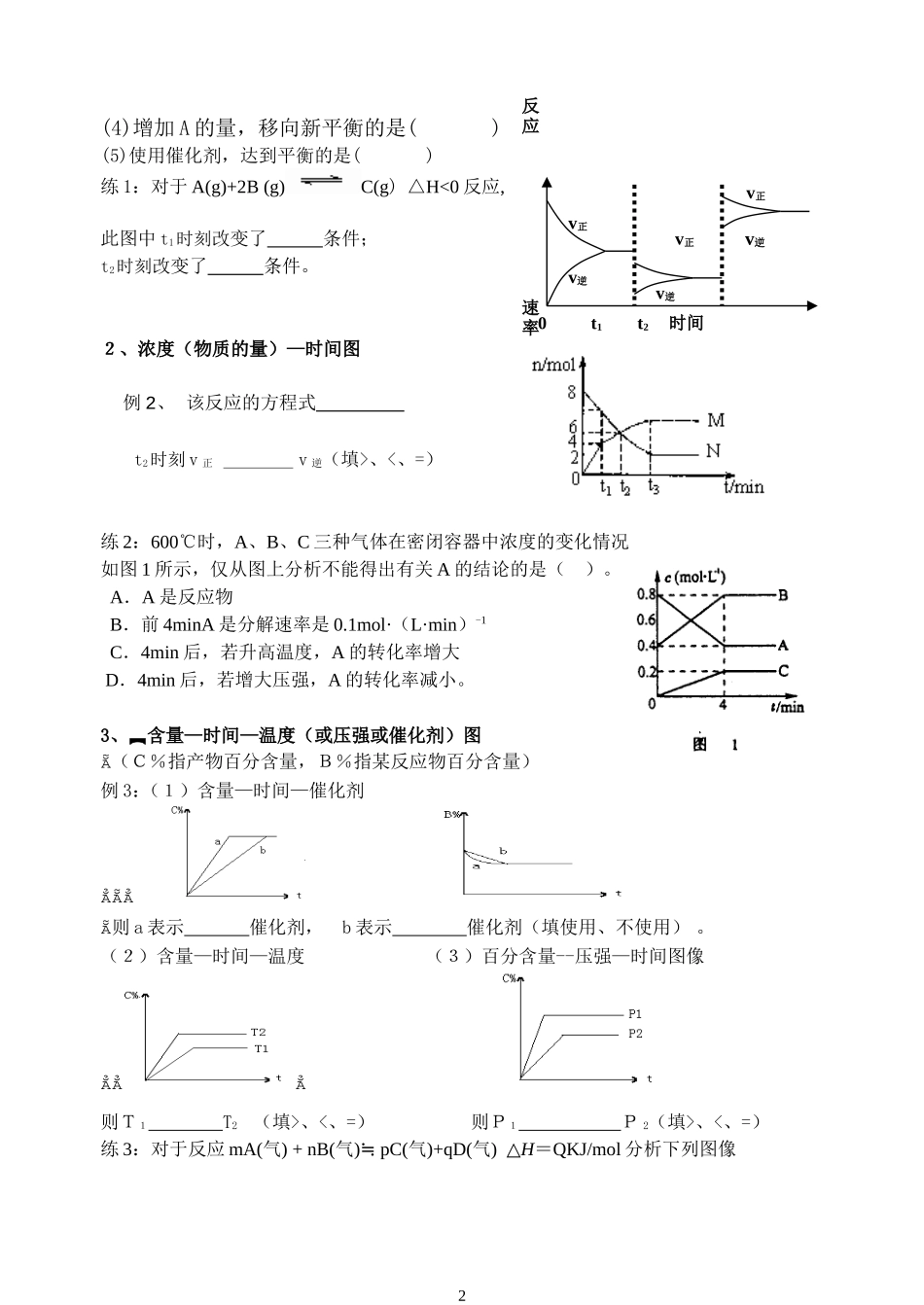
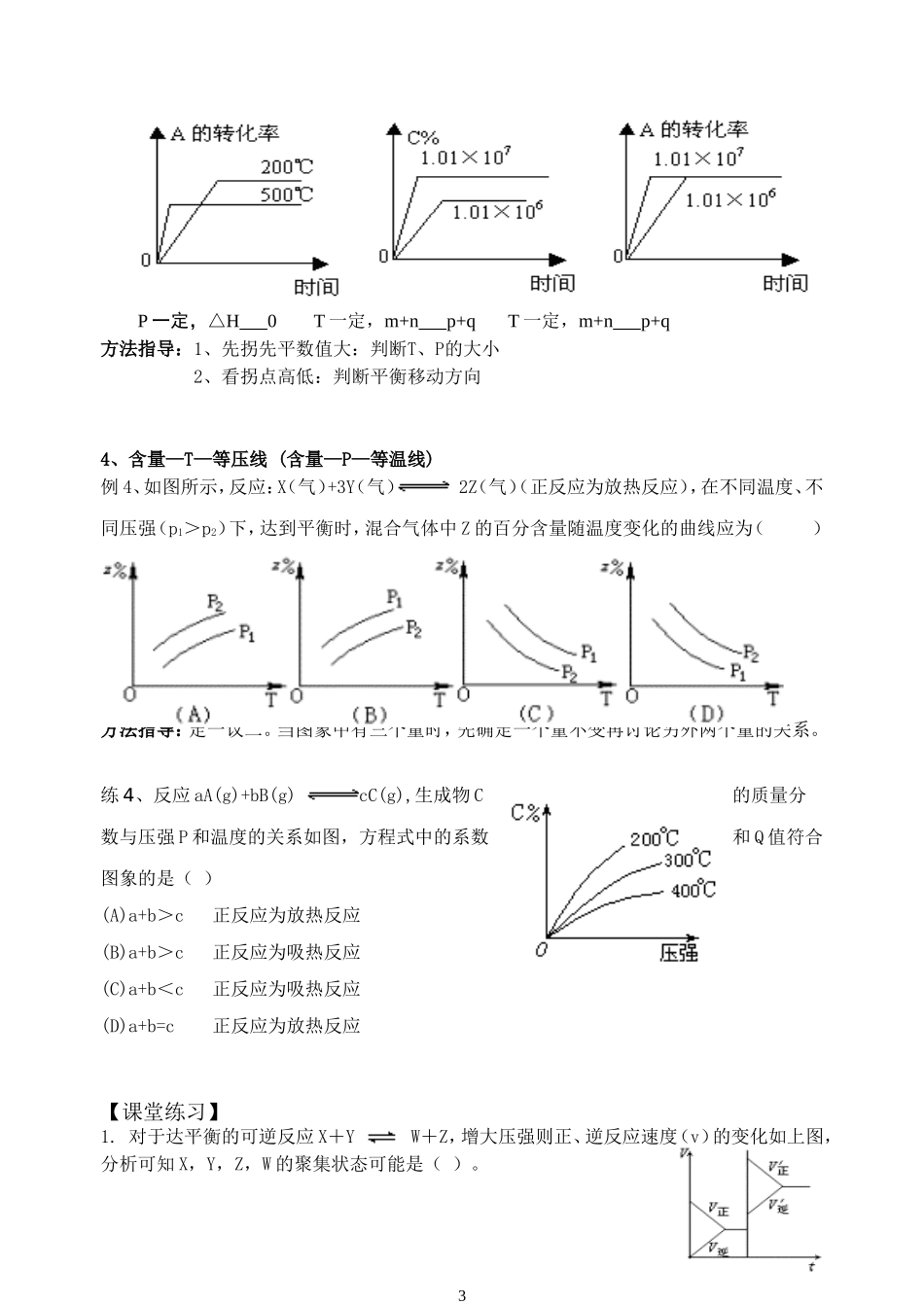
§2-3 化学平衡——图像专题学案【学习目标】1.理解外界条件对化学反应速率和反应限度的影响,认识其一般规律2.掌握解化学平衡图像题的一般方法。【知识回顾】一、影响化学平衡移动及反应速率的因素1.浓度在其他条件不变时,反应物浓度增大或生成物浓度减小,平衡 向移动;反应物浓度减小或生成物浓度增大,平衡 向移动。增大反应物浓度,正反应速率 逆反应速率 (填增大、减小或不变)增大生成物浓度,正反应速率 逆反应速率 减小反应物浓度,正反应速率 逆反应速率 减小生成物浓度,正反应速率 逆反应速率 2.压强对于△v≠0 的可逆反应,在其他条件不变时,增大压强,v 正 v 逆 (填“增大、减小或不变;下同);平衡向 的方向移动;减小压强, v 正 v 逆 ;平衡向 的方向移动。对于△v=0 的可逆反应,在其他条件不变时,增大或减小压强, v 正、v 逆变化的程度 ;所以平衡 移动。3.温度在其他条件不变时,升高温度, v 正 v 逆 (填“增大、减小或不变;下同)平衡向 方向移动;降低温度, v 正 v 逆 ;平衡向 方向移动。4.催化剂由于在其他条件不变时,加入催化剂可以同等程度的改变 反应速率,所以平衡 移动,但是使用催化剂可以改变反应达到平衡的 。【新课学习】二、化学平衡图象的分析思路 一看面:看清图像中横坐标和纵坐标的含义。 二看线:弄清图像中线的斜率或线走势的意义。 三看点:明确曲线的起点、终点、交点及拐点等。 四看是否需要辅助线:等温线,等压线等。 五看量:定量图像中有关量的多少三、化学平衡图象的类型1、速率—时间图 例 1.在一定条件下,反应 A(g)+B(g)C(g)(正反应为放热反应)达到平衡后,根据下列图象判断 A. B. C. D. E.(1)升温,达到新的平衡的是( )(2)降压,达到新的平衡的是( )(3)减少 C 的量,移向新平衡的是( )1反应 速率v逆v正v正v逆v逆0 t1 t2 时间v正(4)增加 A 的量,移向新平衡的是( )(5)使用催化剂,达到平衡的是( )练 1:对于 A(g)+2B (g)C(g) △H<0 反应, 此图中 t1时刻改变了 条件; t2时刻改变了 条件。 2、浓度(物质的量)—时间图 例 2、 该反应的方程式 t2时刻 v 正 v 逆(填>、<、=)练 2:600℃时,A、B、C 三种气体在密闭容器中浓度的变化情况如图 1 所示,仅从图上分析不能得出有关 A 的结论的是( )。A.A 是反应物 B.前 4minA 是分解速率是 0.1mol·(L·min)-1C...