第五单元 化学方程式中考考点清单常考类型剖析实验突破中考考点清单考点一 质量守恒定律 考点二 化学方程式 考点三 利用化学方程式的简单计算(高频考点) 返回总目录考点一 质量守恒定律1
内容:参加化学反应的各物质的 等于反应后生成的各物质的
实质化学反应的过程,就是参加反应的各物质(反应物)的原子重新组合而生成其他物质(生成物)的过程
即在化学反应中,反应前后原子的 没有改变, 没有增减,原子的 也没有改变,因此,化学反应前后物质的总质量守恒
质量总和质量总和种类数目质量中考考点清单3
从宏观和微观角度看质量守恒定律+→ 氢气 + 氧气 → 水 ( H2 ) + ( O2 ) → ( H2O )氢气与氧气反应生成水的示意图中考考点清单 可将化学反应归纳为“五个不变,两个一定改变,两个可能改变”
即:化学反应五个“不变”宏观反应物和生成物的 不变元素 不变微观原子 不变 原子 不变原子 不变两个“一定改变”宏观:物质的种类一定改变微观:分子的种类一定改变两个“可能改变”分子的数目可能改变元素的化合价可能改变总质量种类种类个数质量中考考点清单中考考点清单4 . 质量守恒定律的应用(高频考点)(1) 推断物质的组成
依据:化学反应前后元素种类不变
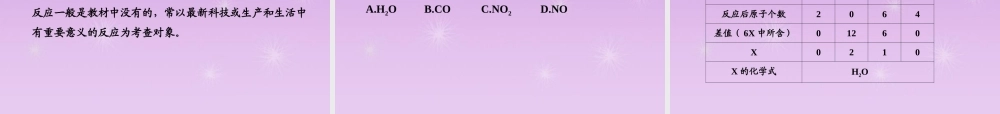
(2) 确定物质的化学式
依据:化学反应前后原子种类、原子数目不变
(3) 推断反应中的化学计量数
依据:化学反应前后原子的数目不变
(4) 解释反应前后物质的质量变化及用质量差确定某一物质的质量
依据:化学反应中,反应物和生成物的总质量不变,原子的质量不变
中考考点清单返回考点目录例题5
质量守恒定律的验证(详见实验突破栏目)中考考点清单考点二 化学方程式1 .定义:用化学式来表示化学反应的式子
2 .表示的意义( 1 )表示反应物、生成物及反应条件
( 2 )表示反应物、生成物之间的质量关系
( 3 )表示反