钠及其化合物连云港市田家炳中学 汤学铃 学习目标• 钠的主要物理性质与化学性质• 钠的氧化物的主要性质• 碳酸钠和碳酸氢钠的性质比较 白:银白色、具有光泽,固体软: 硬度小,很软 [ 易切开、轻压变形 ]轻:密度小, 0
97g/cm3 [ 介于水和煤油之间 ]低: 熔点: 97
81℃ 、沸点: 882
9 ℃[ 低 ] 导:热和电的良导体 ( 原子反应堆的导热剂 )1
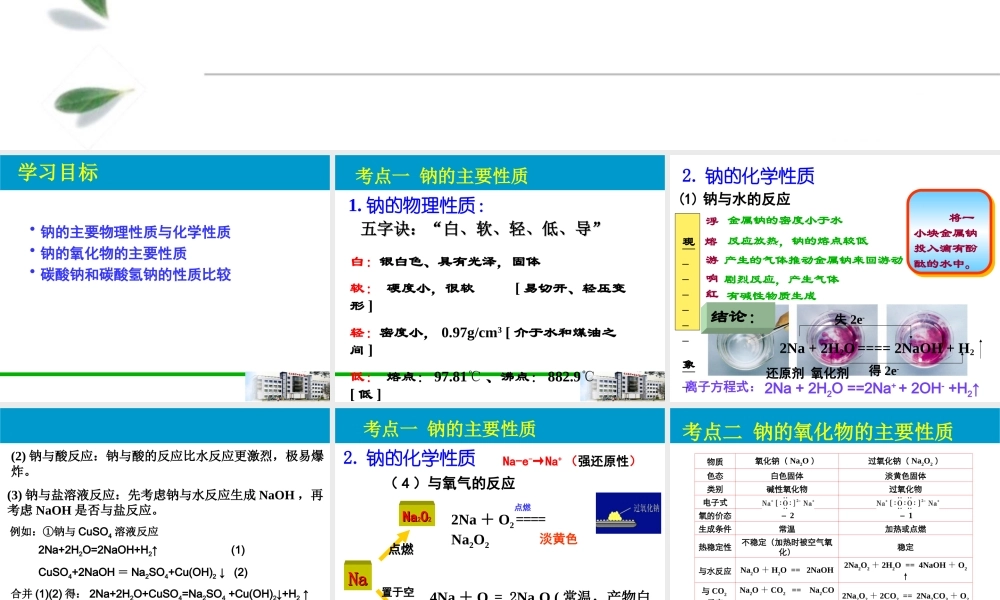
钠的物理性质:五字诀:“白、软、轻、低、导”五字诀:“白、软、轻、低、导”考点一 钠的主要性质(1) 钠与水的反应 将一小块金属钠投入滴有酚酞的水中
现 象 解 释浮游熔响红产生的气体推动金属钠来回游动金属钠的密度小于水反应放热,钠的熔点较低剧烈反应,产生气体有碱性物质生成2Na + 2H2O ==== 2NaOH + H2失 2e-得 2e-还原剂 氧化剂结论:离子方程式: 2Na + 2H2O ==2Na+ + 2OH- +H2↑2
钠的化学性质 (2) 钠与酸反应:钠与酸的反应比水反应更激烈,极易爆炸
(3) 钠与盐溶液反应:先考虑钠与水反应生成 NaOH ,再考虑 NaOH 是否与盐反应
例如:①钠与 CuSO4 溶液反应2Na+2H2O=2NaOH+H2↑ (1)CuSO4+2NaOH = Na2SO4+Cu(OH)2 ↓ (2)合并 (1)(2) 得: 2Na+2H2O+CuSO4=Na2SO4 +Cu(OH)2↓+H2 ↑ 考点一 钠的主要性质2
钠的化学性质Na-e-→Na+ (强还原性)NaNaNaNa22OO22NaNa22OO淡黄色点燃置于空气中4Na + O2 = 2Na2O ( 常温,产物白色 )2Na + O2 ==== Na2O2点燃( 4 )与氧气的反应考点二 钠的氧化物的主要性质物质氧化钠( Na2O )过氧化钠( Na2O2 )色态白色固体淡黄色固体类别碱性氧