第29 讲 价电子对互斥理论、杂化轨道理论及应用 [复习目标] 1
能运用相关的理论来解释或预测简单分子(离子)的空间结构
掌握键角大小原因解释的规范描述
1.价电子对互斥(VSEPR)理论 (1)理论要点 ①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低
②孤电子对排斥力较大,孤电子对越多,排斥力越强,键角越小
(2)价电子对互斥理论推测分子(离子)的空间结构的关键——价电子对数的计算 价电子对数=σ 键电子对数+中心原子的孤电子对数 说明:σ 键电子对数=中心原子结合的原子数;中心原子的孤电子对数=12(a-xb),其中 ①a 表示中心原子的价电子数
对于主族元素:a=原子的最外层电子数
对于阳离子:a=中心原子的价电子数-离子的电荷数
对于阴离子:a=中心原子的价电子数+离子的电荷数(绝对值)
②x 表示与中心原子结合的原子数
③b 表示与中心原子结合的原子最多能接受的电子数(氢为1,其他原子=8-该原子的价电子数
如氧和氧族元素中的S、Se 等均为2,卤族元素均为1)
例如,SOCl2 的空间结构的判断: SOCl2 的中心原子为S,σ 键电子对数为3,孤电子对数为12×(6-1×2-2×1)=1,价电子对数为4,这些价电子对互相排斥,形成四面体形的VSEPR 模型,由于中心原子上有1 个孤电子对,则SOCl2 的空间结构为三角锥形
2.杂化轨道理论 (1)杂化轨道理论概述 中心原子上若干不同类型(主要是s、p 轨道)、能量相近的原子轨道混合起来,重新组合成同等数目、能量完全相同的新轨道
杂化轨道数不同,轨道间的夹角不同,形成分子的空间结构不同
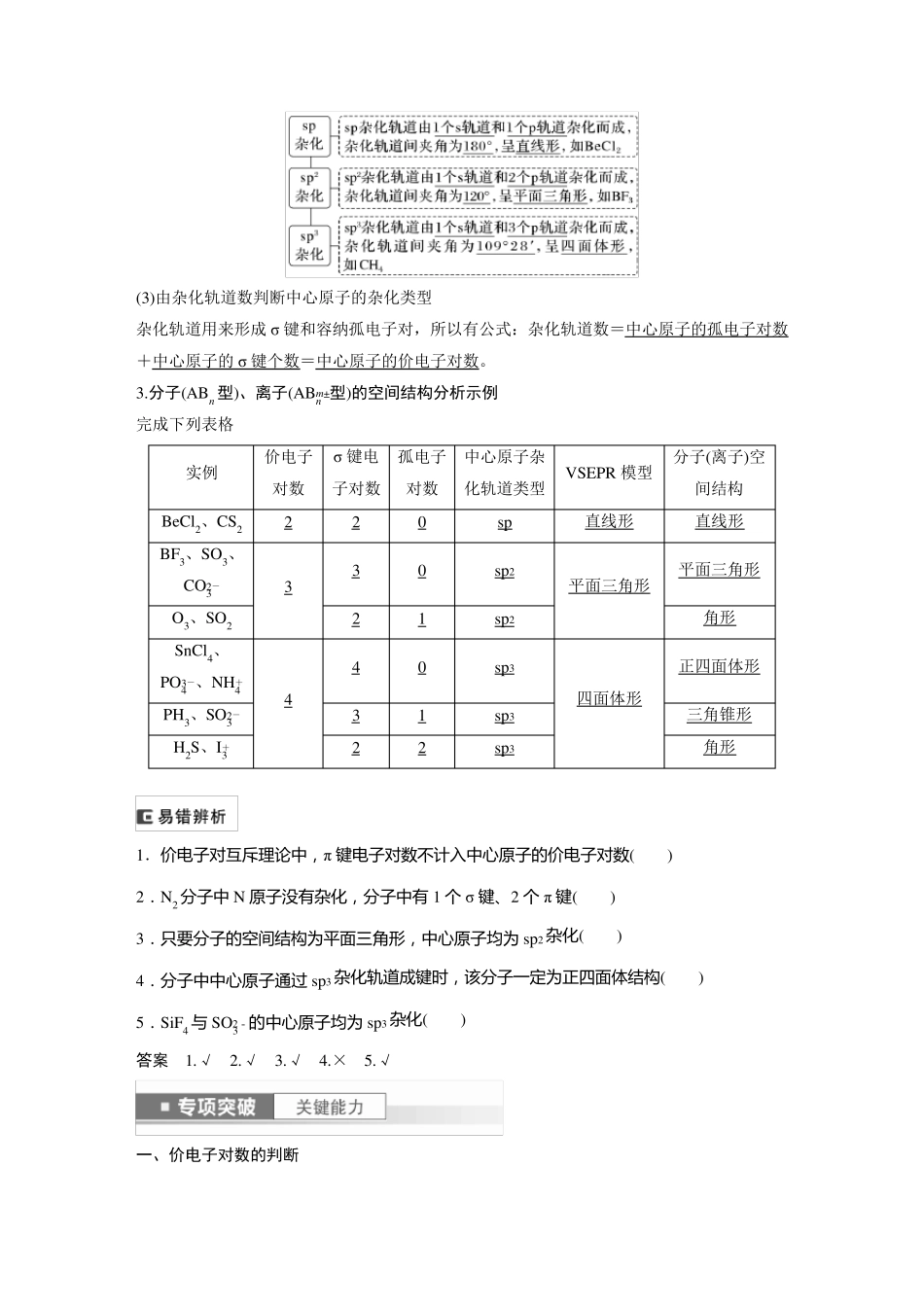
(2)杂化轨道三种类型 (3)由杂化轨道数判断中心原子的杂化类型 杂化轨道用来形成σ 键和容纳孤电子对,所以有公式:杂化轨道数=中心原子的孤电子对数+中心原子的σ 键个数=中心原子的价