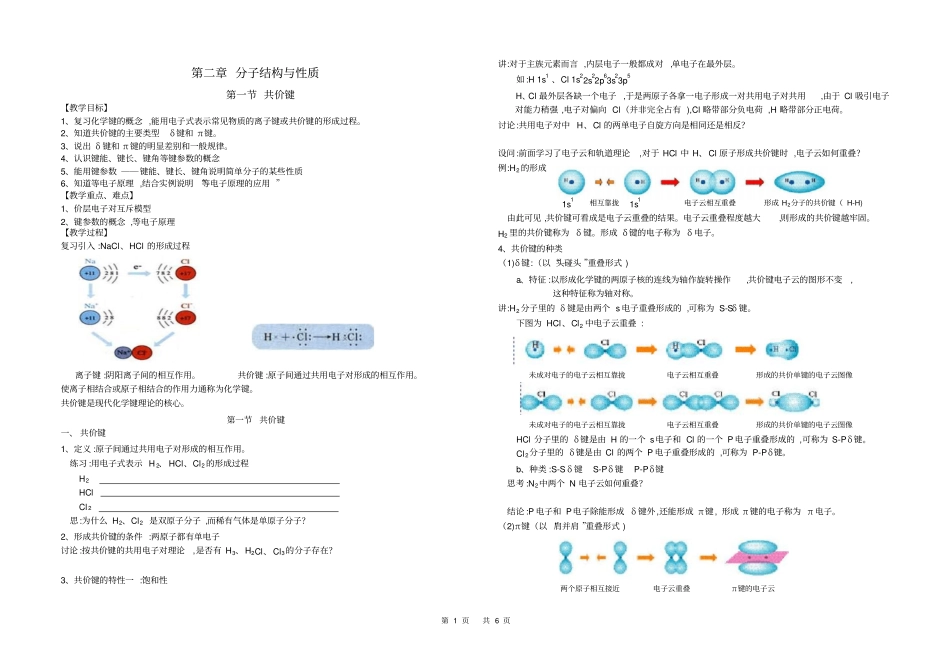
第 1 页共 6 页第二章 分子结构与性质第一节 共价键【教学目标】1、复习化学键的概念 ,能用电子式表示常见物质的离子键或共价键的形成过程
2、知道共价键的主要类型δ 键和 π 键
3、说出 δ 键和 π 键的明显差别和一般规律
4、认识键能、键长、键角等键参数的概念5、能用键参数 ――键能、键长、键角说明简单分子的某些性质6、知道等电子原理 ,结合实例说明 “等电子原理的应用 ”【教学重点、难点】1、价层电子对互斥模型2、键参数的概念 ,等电子原理【教学过程】复习引入 :NaCl、HCl 的形成过程离子键 :阴阳离子间的相互作用
共价键 :原子间通过共用电子对形成的相互作用
使离子相结合或原子相结合的作用力通称为化学键
共价键是现代化学键理论的核心
第一节 共价键一、 共价键1、定义 :原子间通过共用电子对形成的相互作用
练习 :用电子式表示 H 2、 HCl、Cl2 的形成过程H2 HCl Cl 2 思:为什么 H2、Cl2 是双原子分子 ,而稀有气体是单原子分子
2、形成共价键的条件 :两原子都有单电子讨论 :按共价键的共用电子对理论,是否有 H3、H2Cl、Cl3的分子存在
3、共价键的特性一 :饱和性讲:对于主族元素而言 ,内层电子一般都成对 ,单电子在最外层
如:H 1s1 、Cl 1s22s22p63s23p5 H、Cl 最外层各缺一个电子 ,于是两原子各拿一电子形成一对共用电子对共用,由于 Cl 吸引电子对能力稍强 ,电子对偏向 Cl(并非完全占有 ),Cl 略带部分负电荷 ,H 略带部分正电荷
讨论:共用电子对中 H、Cl 的两单电子自旋方向是相同还是相反
设问:前面学习了电子云和轨道理论,对于 HCl 中 H、Cl 原子形成共价键时 ,电子云如何重叠
例:H2 的形成1s1 相互靠拢1s1 电子云相互重叠形成 H2分子的共价键( H-H)由此可见 ,共