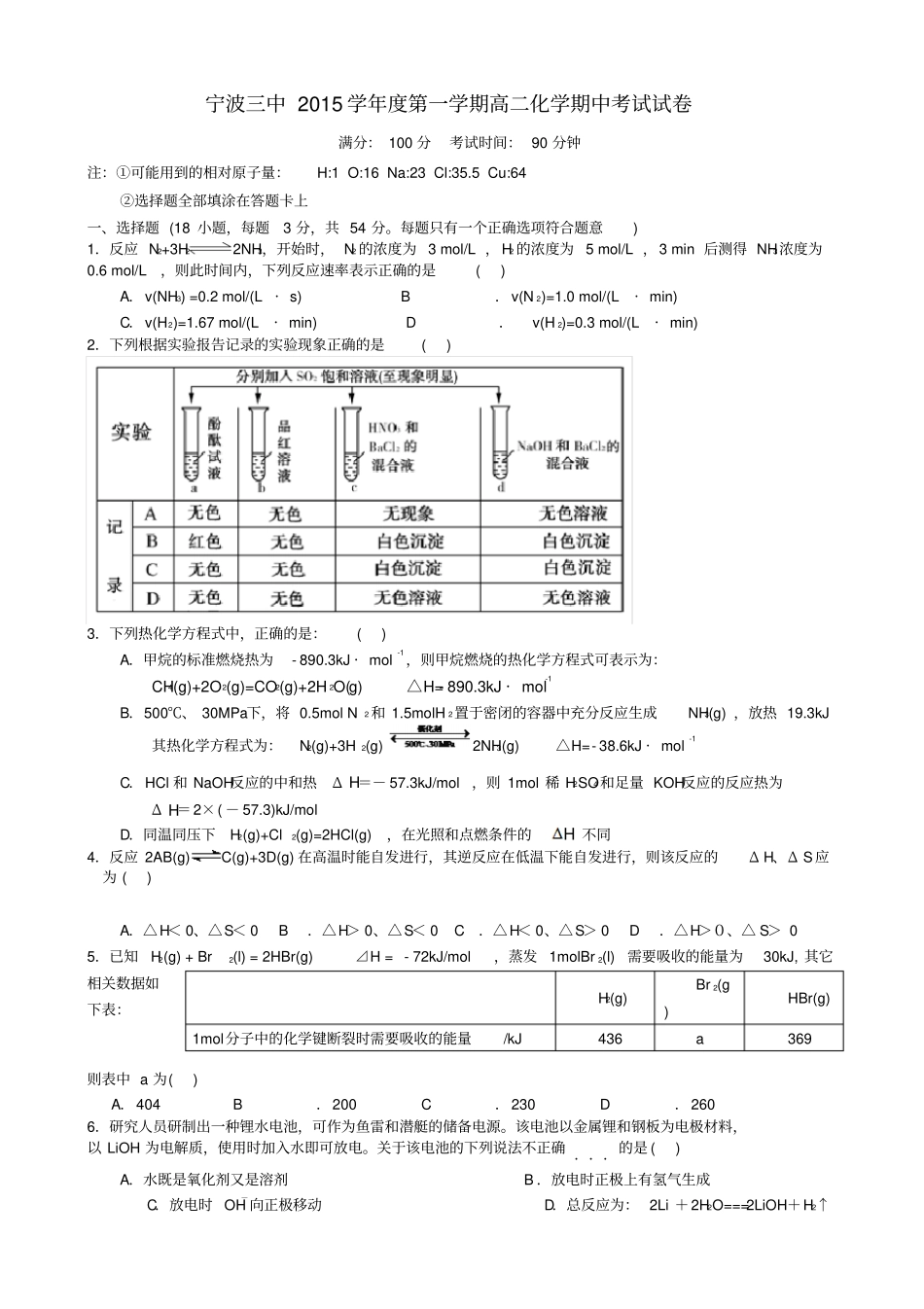
宁波三中 2015 学年度第一学期高二化学期中考试试卷满分: 100 分考试时间: 90 分钟注:①可能用到的相对原子量:H:1 O:16 Na:23 Cl:35.5 Cu:64 ②选择题全部填涂在答题卡上一、选择题 (18 小题,每题3 分,共 54 分。每题只有一个正确选项符合题意) 1.反应 N2+3H22NH3,开始时, N2 的浓度为 3 mol/L ,H2 的浓度为 5 mol/L ,3 min 后测得 NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是 ( ) A.v(NH3) =0.2 mol/(L· s) B.v(N 2)=1.0 mol/(L· min)C.v(H2)=1.67 mol/(L· min) D.v(H 2)=0.3 mol/(L· min)2.下列根据实验报告记录的实验现象正确的是( ) 3.下列热化学方程式中,正确的是:( ) A.甲烷的标准燃烧热为- 890.3kJ · mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H 2O(g) △H=- 890.3kJ · mol-1 B.500℃、 30MPa下,将 0.5mol N2 和 1.5molH 2置于密闭的容器中充分反应生成NH3(g) ,放热 19.3kJ 其热化学方程式为:N2(g)+3H 2(g)2NH3(g) △H=- 38.6kJ · mol-1 C.HCl 和 NaOH反应的中和热Δ H=- 57.3kJ/mol,则 1mol 稀 H2SO4 和足量 KOH反应的反应热为Δ H=2×( - 57.3)kJ/mol D.同温同压下H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件的H 不同4.反应 2AB(g)C(g)+3D(g) 在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的Δ H、Δ S应为 ( ) A.△H< 0、△S< 0 B.△H> 0、△S< 0 C.△H< 0、△S> 0 D.△H>0、△ S> 0 5.已知H2(g) + Br2(l) = 2HBr(g) ⊿H = - 72kJ/mol ,蒸发 1molBr 2(l)需要吸收的能量为30kJ, 其它相关数据如下表:则表中 a 为( ) A.404 B.200 C.230 D.260 6.研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以 LiOH 为电解质,使用时加入水即可放电。关于该电池的下列说法不正确 ...的是 ( ) A.水既是氧化剂又是溶剂 B .放电时正极上有氢气生成C.放电时 OH-向正极移动D.总反应为: 2Li +2H2O=== 2LiOH+H2↑H2(g) Br 2(g) HBr(g) 1mol分子中的化学键断裂时需要吸收的能量/kJ 436 a 369 27.生物燃料电池(BFC) 是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿...