第 1 页 共 1 2 页 高二化学实验专题 一、中和热及其实验测定 1.50 mL 0
50 mol·L-1盐酸与 50 mL 0
55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应
通过测定反应过程中所放出的热量可计算中和反应的反应热
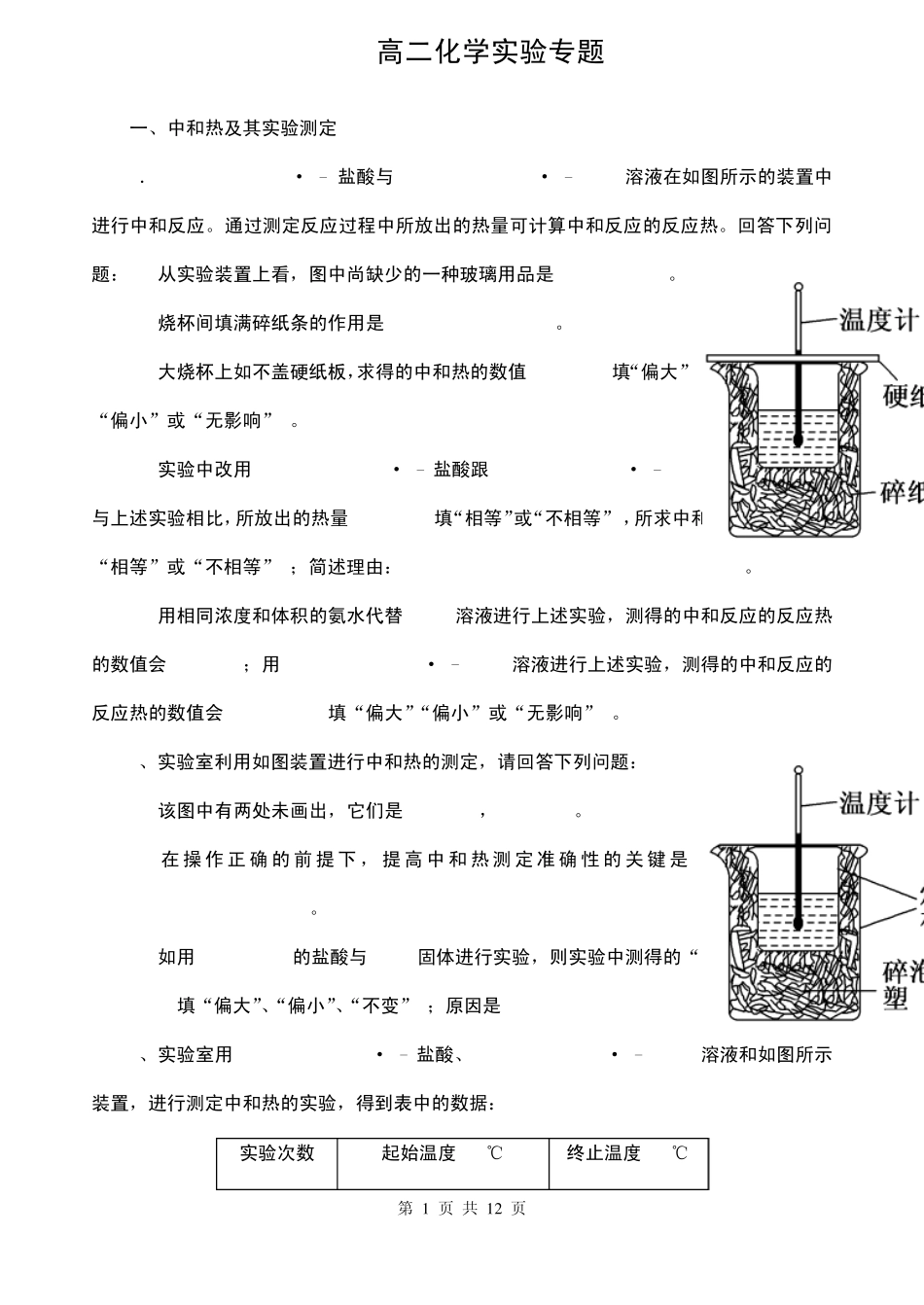
回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是____________
(2)烧杯间填满碎纸条的作用是__________________
(3)大烧杯上如不盖硬纸板,求得的中和热的数值________(填“偏大”“偏小”或“无影响”)
(4)实验中改用 60 mL 0
50 mol·L-1盐酸跟 50 mL 0
55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”);简述理由:____________________________________
(5)用相同浓度和体积的氨水代替 NaOH溶液进行上述实验,测得的中和反应的反应热的数值会________;用 50 mL 0
50 mol·L-1NaOH溶液进行上述实验,测得的中和反应的反应热的数值会__________(填“偏大”“偏小”或“无影响”)
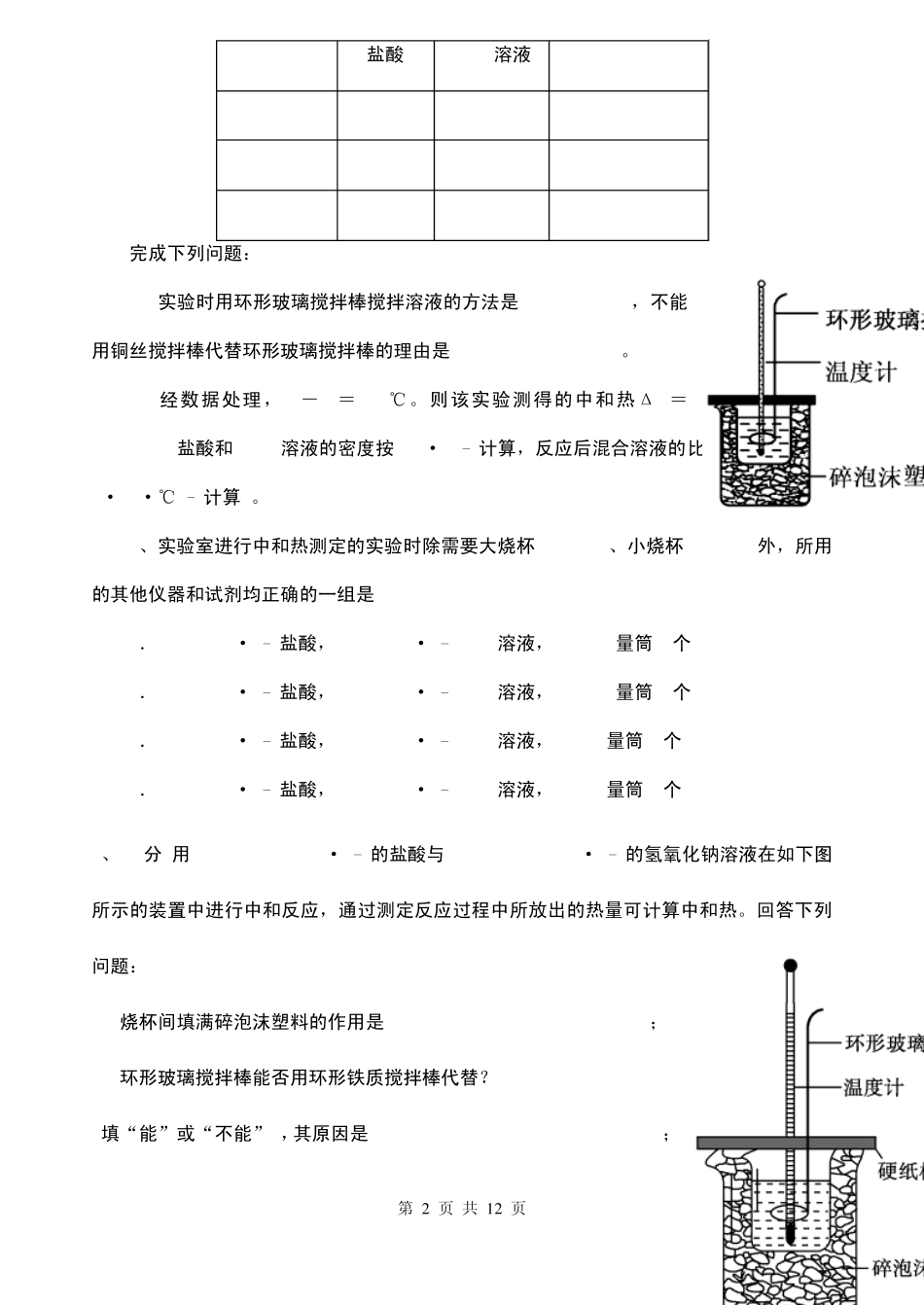
2、实验室利用如图装置进行中和热的测定,请回答下列问题: (1)该图中有两处未画出,它们是________,________
(2)在 操 作 正 确 的 前 提 下 , 提 高中和热测定准 确 性 的 关 键 是_______________________
(3)如用 0
5 mol/L的盐酸与 NaOH固体进行实验,则实验中测得的“中和热”数值将________(填“偏大”、“偏小”、“不变”);原因是__________________________________