1 初中化学综合计算题及详细分析 相对原子质量:H—1 C—12 O 一 16 Cl—35
5 Zn—65 Ca—40 Na 一 23 K—39 Mg—24、Fe—56、 1、将 29
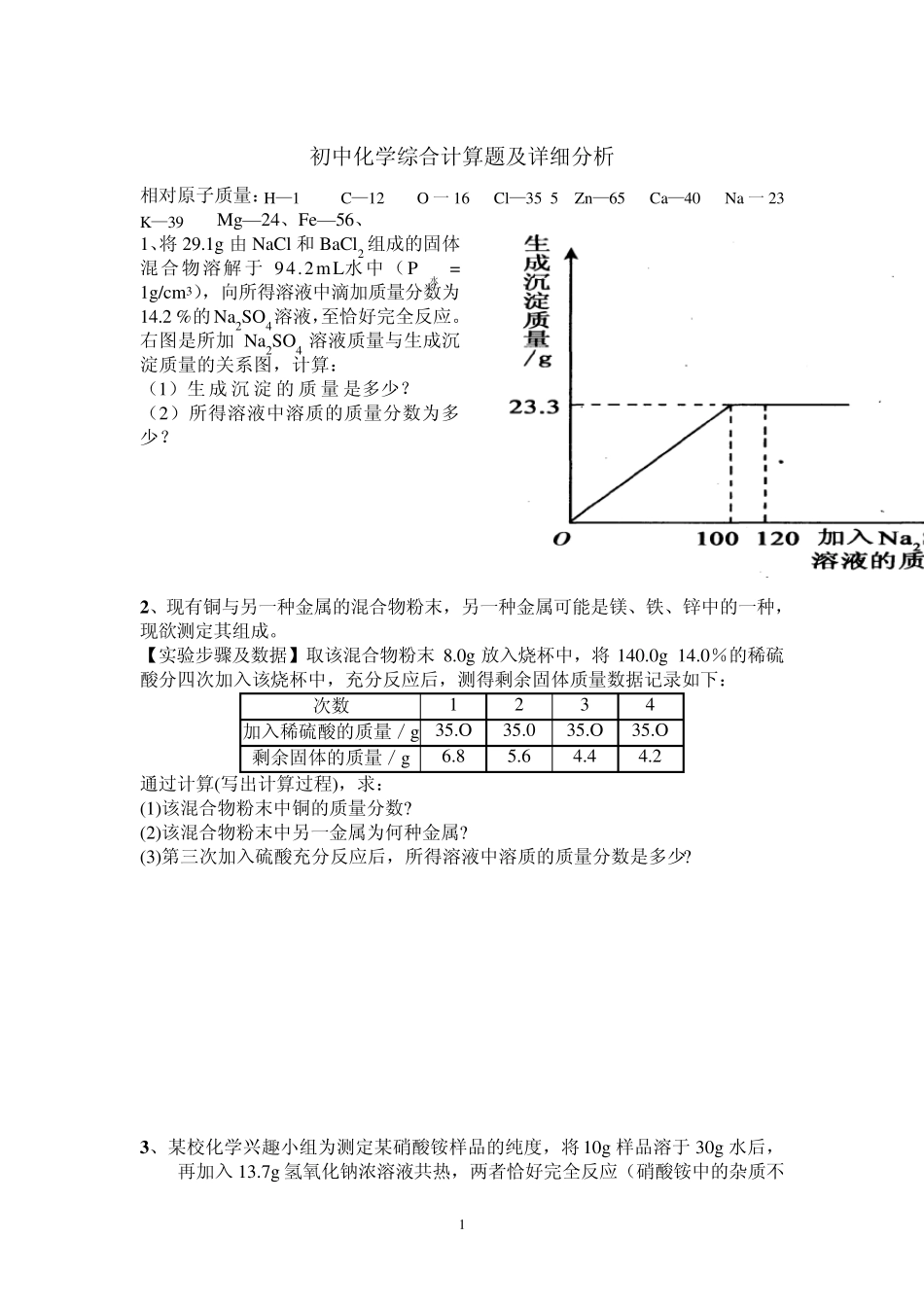
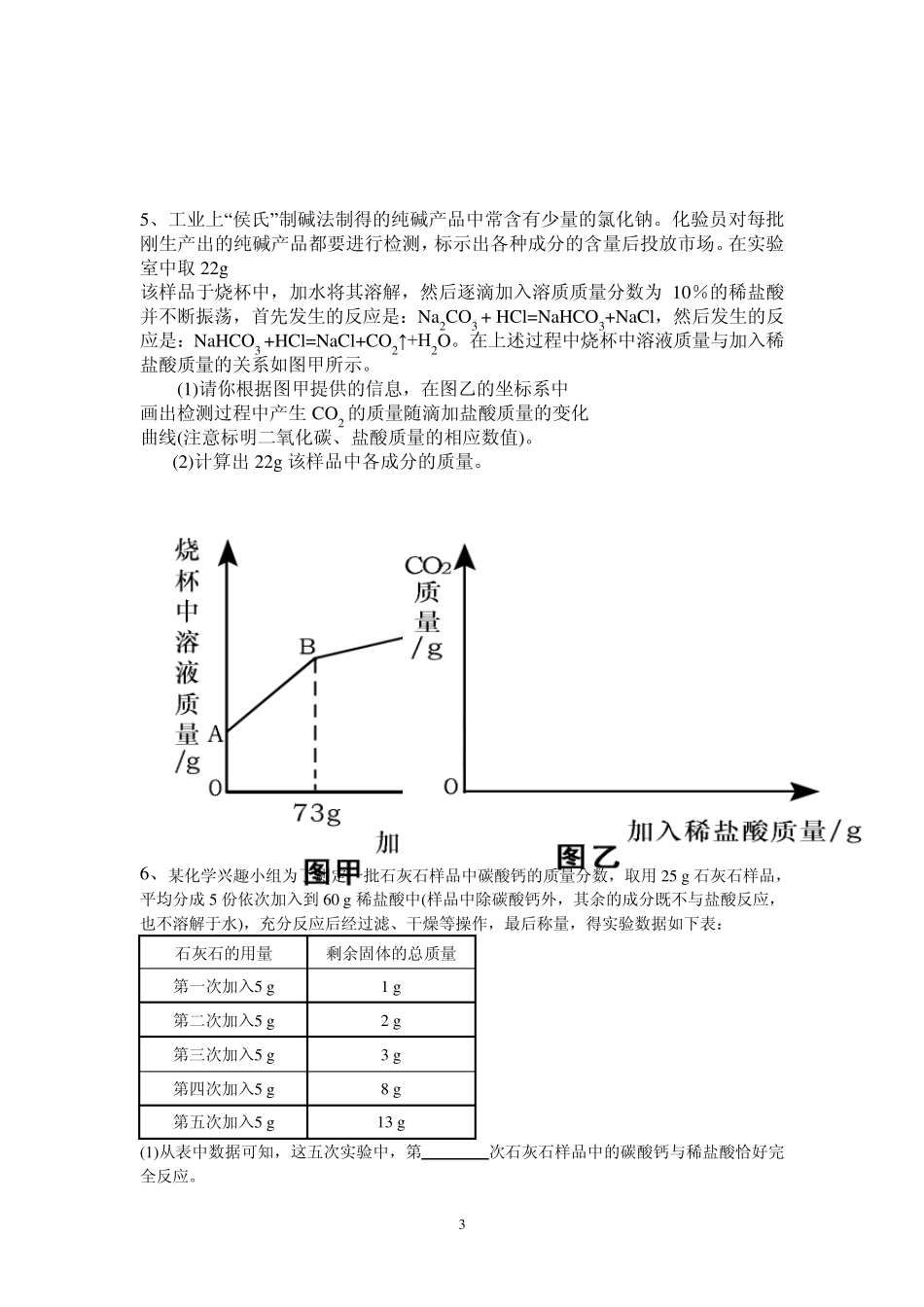
1g 由 NaCl 和 BaCl2 组成的固体混合物溶解于 94
2mL水中(P水 = 1g/cm3),向所得溶液中滴加质量分数为14
2 %的Na2SO4溶液,至恰好完全反应
右图是所加 Na2SO4 溶液质量与生成沉淀质量的关系图,计算: (1)生 成 沉 淀 的 质量是多少
(2)所得溶液中溶质的质量分数为多少
2 、现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成
【实验步骤及数据】取该混合物粉末 8
0g 放入烧杯中,将 140
0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下: 次数 1 2 3 4 加入稀硫酸的质量/g 35
O 剩余固体的质量/g 6
2 通过计算(写出计算过程),求: (1)该混合物粉末中铜的质量分数
(2)该混合物粉末中另一金属为何种金属
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少
3 、某校化学兴趣小组为测定某硝酸铵样品的纯度,将 10g 样品溶于 30g 水后,再加入 13
7g 氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不 2 与氢氧化钠反应,也不溶于水,硝酸铵与氢氧化钠的反应方程式为:NH4NO3+NaOH 加热NaNO3+H2O+NH3↑)
把产生的所有NH3 用足量的硫酸溶液吸收,同时测量2 分钟内硫酸溶液增加的质量,结果如下表所示: 时间/s 0 20 30 40 60 80 100 120 增加的质量/g 0 0
7 试回答下列问题: