四元环的合成四元环特别难于合成,他们约有90度的键角张力,四元环有时也可以通过普通的关环方法得到
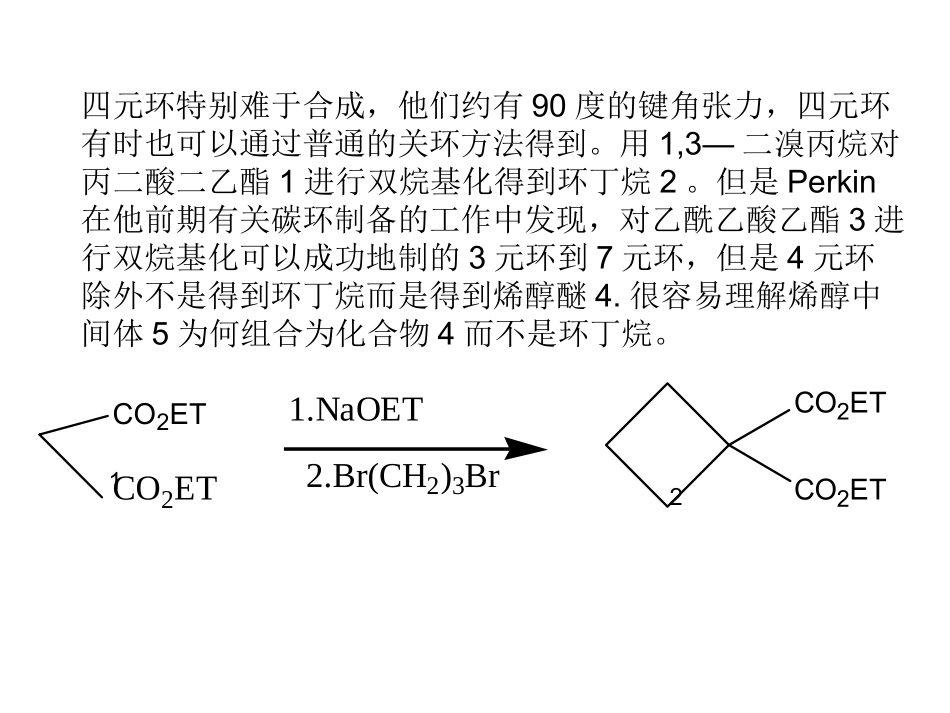
用1,3—二溴丙烷对丙二酸二乙酯1进行双烷基化得到环丁烷2
但是Perkin在他前期有关碳环制备的工作中发现,对乙酰乙酸乙酯3进行双烷基化可以成功地制的3元环到7元环,但是4元环除外不是得到环丁烷而是得到烯醇醚4
很容易理解烯醇中间体5为何组合为化合物4而不是环丁烷
CO2ETCO2ET1
NaOET2
Br(CH2)3BrCO2ETCO2ET12CO2ETO1
NaOET2
Br(CH2)3BrOCO2ETBrOCO2ET345光化学合成我们已经意识到Diels-Alder反应非常容易进行,当双烯体6与亲烯体7一起加热是能形成六元环化合物,为什么四元环9不能生成呢
这是因为轨道对称性要求环加成需要6个π电子参与,而不是四个π参与
CO2ET4+2»·¼Ó³ÉCO2ETCO2ET2+2»·¼Ó³ÉCO2ET67892+2环加成要求在激发态下发生,而这就是光化学反应,如果一种组分吸收了光能形成激发态,而另一组分处于基态,那么他们的光化学反应是最匹配的,即便是乙烯也可以和共轭烯酮10在光辐射反应得到环丁烷11
+OhvOH1011两个组分都可以是官能团化的,这使得切断化合物12的中间环化大大简化,仅需要两个简单的化合物13和14,对混合物进行光辐射能得到化合物12,且收率很好,121314OCO2ETCO2ET2+2O+MeO2CMeO2C大多数的环丁烷化合物能提供两种2+2切断可供选择,至于选择何种方法则往往视起始原料的易得性决定
从化合物11可知,此类化合物能通过光照射乙烯和烯酮(如15)而得到,因此,我们光柱另一条路线B
其分子内的光环加成的起始原料应该是烯酮17,由于醇18易获得,17可以由18氧化而得到
2+2bOHOFGI15161718O+2+2aHHababO醇18