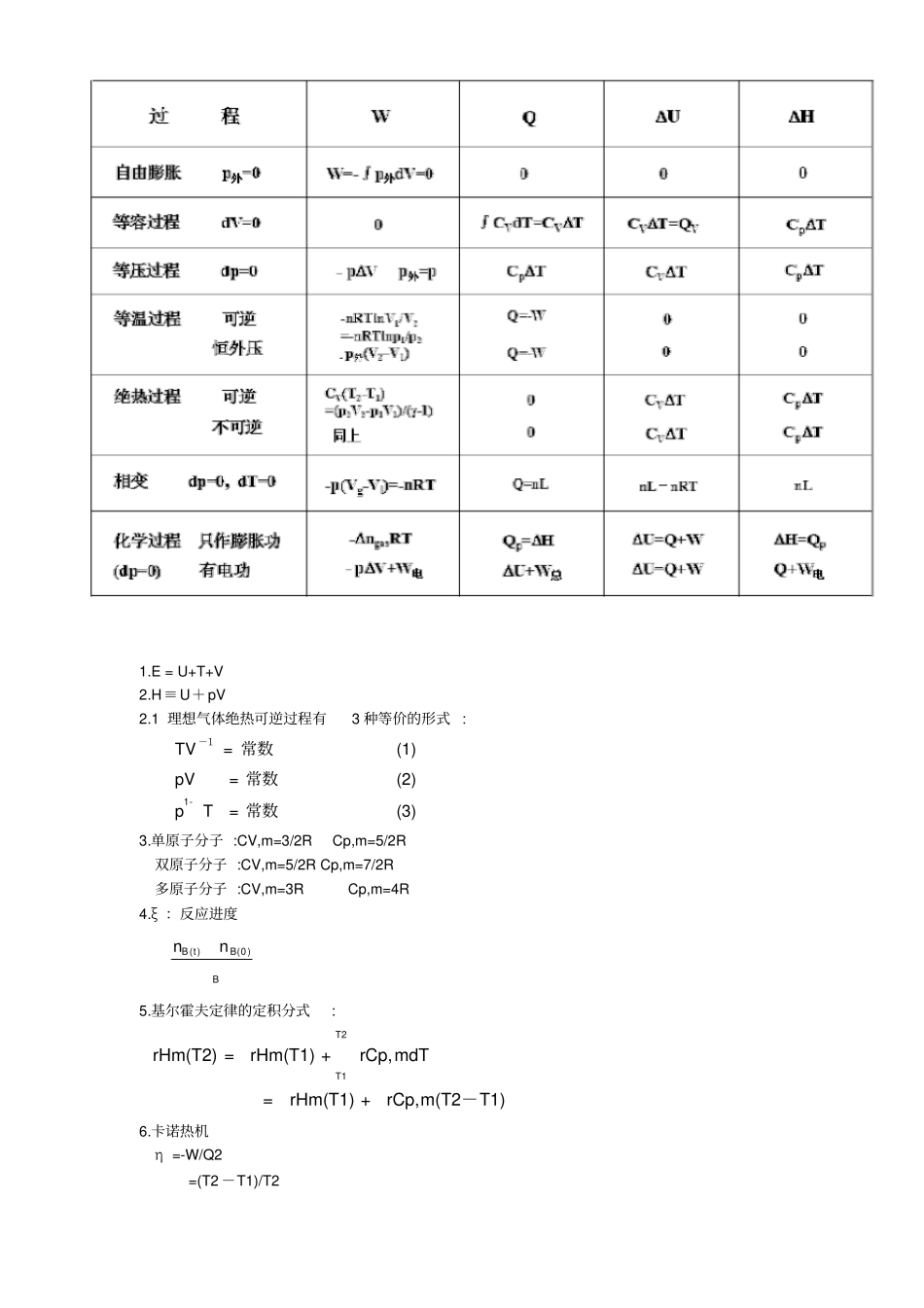
E = U+T+V 2
H≡U+pV 2
1 理想气体绝热可逆过程有3 种等价的形式 : (3)常数=Tp(2)常数=pV(1)常数=TV-1-13
单原子分子 :CV,m=3/2R Cp,m=5/2R 双原子分子 :CV,m=5/2R Cp,m=7/2R 多原子分子 :CV,m=3R Cp,m=4R 4
ξ :反应进度BBtBnn)0()(5
基尔霍夫定律的定积分式: T1)-m(T2rCp,+rHm(T1)=mdTrCp,+rHm(T1)=rHm(T2)T2T16
卡诺热机η =-W/Q2 =(T2 -T1)/T2 =1-(T1/T2) 7
熵的微观意义:S=klnW W:宏观状态拥有的微观运动状态的数量k:Boltzmann 常数8
纯物质 B 在状态 (T,p) 的规定熵即为下述过程的熵变 : ),()0(pTBKBKpTBTKpTBSSSS0,0),(9
等温过程的熵变: (理想气体 ) (p1/p2)nRln =Sp2/p1=V2/V1∴p2V2=p1V1 (1)(V2/V1)nRln =S1)/TnRTln(V2/V=-WR/T=QR/T=QR/T∫=S10
绝热过程 : 绝热可逆过程 , 由熵的判别式 : 0=S绝热可逆(2) 绝热不可逆过程: 对此类过程需设计一条可逆途径, 从相同的始态到相同末态, 再沿可逆途径求算熵变
变温过程 : 简单体系A
等压变温 : )Cpln(T2/T1=(4)(Cp/T)dT=QR/T∫=SCpdT=QRB
等容变温 : ln(T2/T1)C=/T)dT∫(C=/TQ∫=SdTC=QVVRVR12
相变过程:平衡相变:平衡相变是一可逆过程, 在等温等压下进行
/TQ=Q/T∫=SR平衡相变有 : H=Qp故平衡相变的熵变为: 相变H/T=S(6) 即:平衡相变的熵变等于相变潜热除以相变温度13