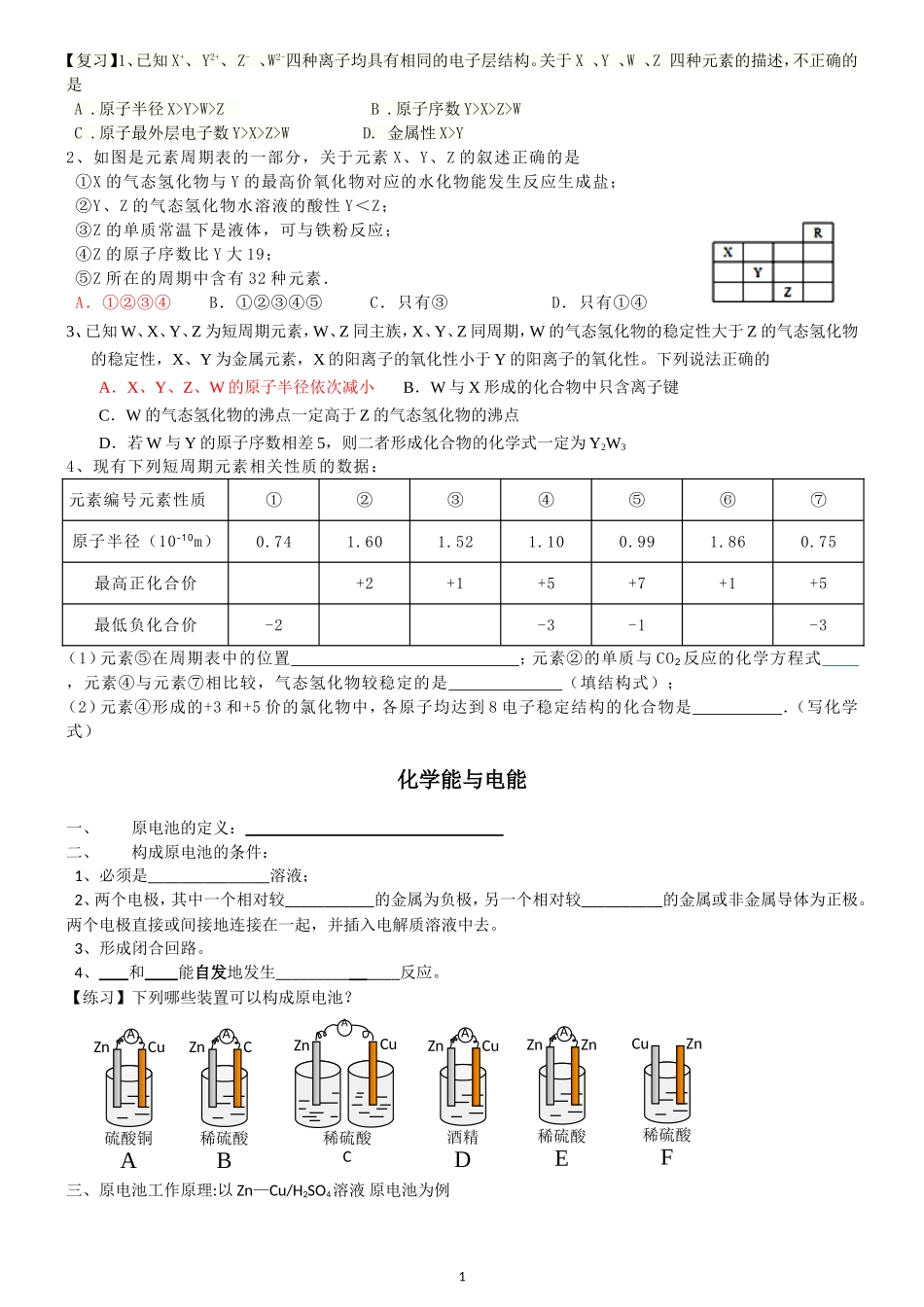
【复习】1、已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。关于X、Y、W、Z四种元素的描述,不正确的是A.原子半径X>Y>W>ZB.原子序数Y>X>Z>WC.原子最外层电子数Y>X>Z>WD.金属性X>Y2、如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐;②Y、Z的气态氢化物水溶液的酸性Y<Z;③Z的单质常温下是液体,可与铁粉反应;④Z的原子序数比Y大19;⑤Z所在的周期中含有32种元素.A.①②③④B.①②③④⑤C.只有③D.只有①④3、已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的A.X、Y、Z、W的原子半径依次减小B.W与X形成的化合物中只含离子键C.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W34、现有下列短周期元素相关性质的数据:元素编号元素性质①②③④⑤⑥⑦原子半径(10-10m)0.741.601.521.100.991.860.75最高正化合价+2+1+5+7+1+5最低负化合价-2-3-1-3(1)元素⑤在周期表中的位置;元素②的单质与CO2反应的化学方程式,元素④与元素⑦相比较,气态氢化物较稳定的是(填结构式);(2)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是.(写化学式)化学能与电能一、原电池的定义:二、构成原电池的条件:1、必须是_______________溶液;2、两个电极,其中一个相对较___________的金属为负极,另一个相对较__________的金属或非金属导体为正极。两个电极直接或间接地连接在一起,并插入电解质溶液中去。3、形成闭合回路。4、和能自发地发生_____________反应。【练习】下列哪些装置可以构成原电池?三、原电池工作原理:以Zn—Cu/H2SO4溶液原电池为例1硫酸铜AAZnCu稀硫酸BAZnC酒精DAZnCu稀硫酸EAZnZn稀硫酸CZnCuA稀硫酸FCuZn外电路:电子流向:电流流向:内电路:阳离子→极阴离子→极【考点】判断判断原电池正、负极的方法由组成原电池的两极材料判断:根据电流方向或电子流动方向判断:根据原电池两极发生的变化来判断:【练习】1.下列说法正确的是A.原电池是把电能转化为化学能的装置B.原电池中电子流出的一极是正极,发生氧化反应C.原电池中的阳离子向正极移动D.原电池两极均发生氧化还原反应2.关于铜—锌—稀硫酸构成的原电池的有关叙述错误的是A.锌为负极,锌发生氧化反应B.铜为正极,铜不易失去电子而受到保护C.负极发生还原反应,正极发生氧化反应D.外电路电子流入的一极为正极,电子流出的一极为负极3.将锌片和铜片用导线连接平行插入同一稀硫酸溶液中,下列叙述正确的是()A.正极附近硫酸根离子的浓度逐渐增大B.负极附近硫酸根离子浓度逐渐增大C.正极、负极硫酸根离子的浓度基本不变D.正极附近硫酸根离子的浓度逐渐减小4.某原电池总反应是Zn+Cu2+=Zn2++Cu,该原电池组成及判断正确的是()ABCD正极ZnCuZnCu负极CuZnCuZn电解质溶液CuCl2CuCl2ZnCl2ZnCl2【考点】电极反应式的书写①Mg—Al/H2SO4②Mg—Al/NaOH③Cu—C/AgNO3④Fe—Cu/FeCl3⑤Fe—C/NaCl四、原电池的应用①制作化学电源②加快反应速率:如,实验室制H2时,由于锌太纯,反应一般较慢,可加入少量CuSO4以加快反应速率。③判断金属活动性的强弱④防止金属的腐蚀。【练习】1、把a、b、c、d4块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,d极上产生大量气泡;a、c相连时,电流由c经导线流向a;b、d相连电子由d经导线流向b,则此4种金属的活动性由强到弱的顺序为()A.a>b>c>dB.a>c>d>bC.c>a>b>dD.b>d>c>a2、X、Y、Z都是金属,把X浸入Z的硝酸溶液中,X的表面有Z析出,X与Y组成原电池时,Y为负极。X、Y、Z三种金属的活动性顺序为()A、X>Y>ZB、X>Z>YC、Y>X>ZD、Y>Z>X3、如右图所示,如果电流计偏转,a变粗,b变细,符合这种情况的是A.a是锌,b是铜,c是硫酸溶液B.a是铁,b是银,c是硝酸银溶液2项目ZnCu电极反应电子得...