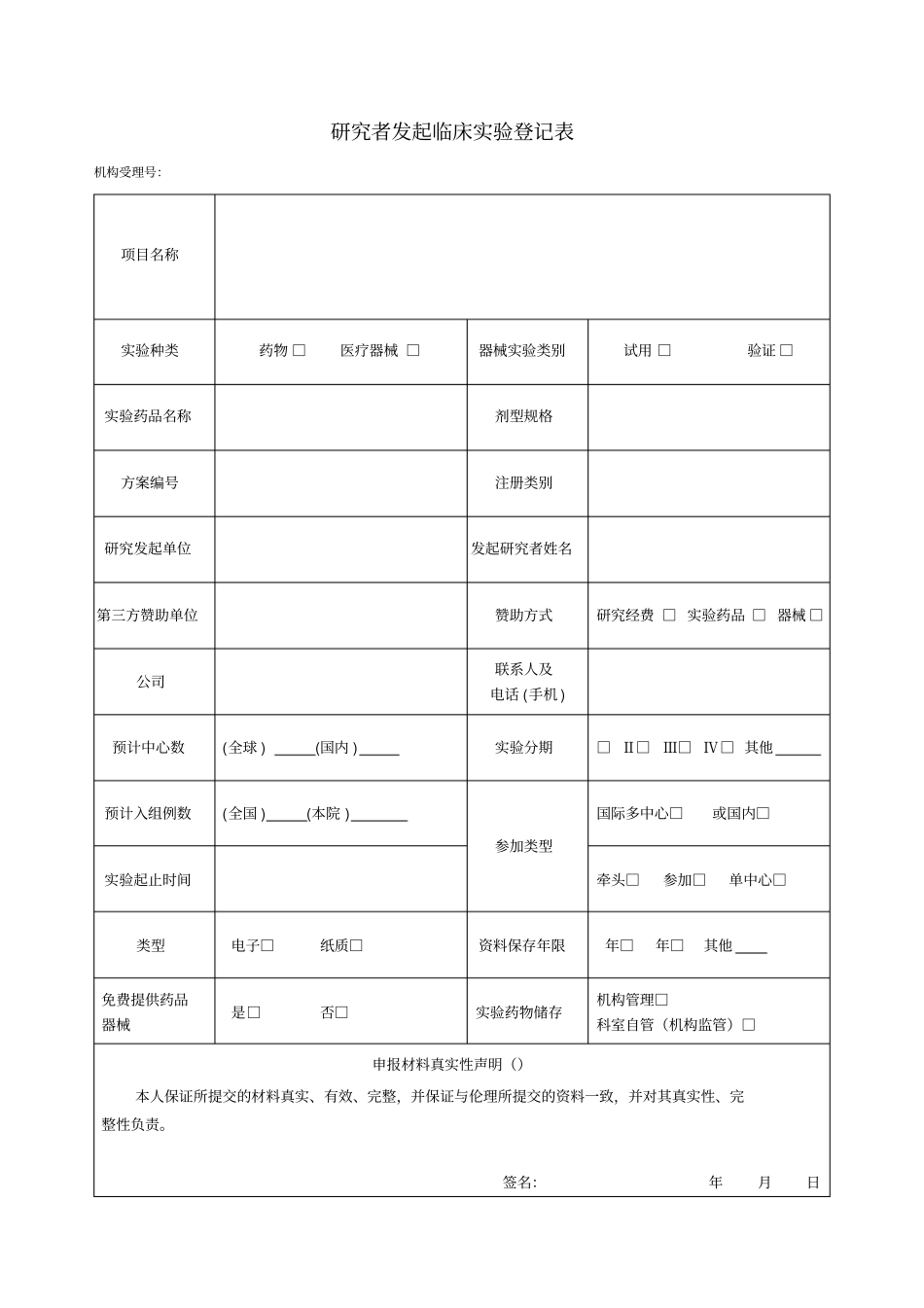
研究者发起临床实验登记表机构受理号:项目名称实验种类药物 □医疗器械 □器械实验类别试用 □验证 □实验药品名称剂型规格方案编号注册类别研究发起单位发起研究者姓名第三方赞助单位赞助方式研究经费 □ 实验药品 □ 器械 □公司联系人及电话 (手机 ) 预计中心数(全球 ) (国内 ) 实验分期□ Ⅱ□Ⅲ□ Ⅳ□ 其他预计入组例数(全国 ) (本院 ) 参加类型国际多中心□或国内□实验起止时间牵头□参加□单中心□类型电子□纸质□资料保存年限年□年□其他免费提供药品器械是□否□实验药物储存机构管理□科室自管(机构监管)□申报材料真实性声明()本人保证所提交的材料真实、有效、完整,并保证与伦理所提交的资料一致,并对其真实性、完整性负责
签名:年月日研究团队成员:姓名职称项目分工是否获得证书签名联系电话主要研究者声明本人自觉接受国家有关法律和法规的约束,对该项目的所有临床研究资料及相关内容保密,保护受试者权益及隐私,并郑重承诺与该项目无任何利益冲突
本人已审阅所有临床实验资料,认为本科室的人员配备、病源量和设备条件满足该项目实验要求,团队成员有充分的时间、并保证在约定时间内入组完成实验
本人同意并确认上述人员参加该临床实验
主要研究者签字:年月日(下表由机构填写)机构意见: 经形式审查资料合格
审查人签字:年月日注:
团队成员中必须授权项目质控员名,负责该项目的质控工作
研究团队成员必须经过培训
机构登记表正反面打印
所有选择项目的“□”内用“×”标注