第二单元微粒之间的相互作用力课 时 1 离 子 键【我思我学】议一议: 构成物质的基本微粒有哪几种
分别举例说明
想一想: 不同的物质含有不同的微粒,这些微粒是如何彼此结合而构成物质的
议一议: 为什么氢原子与氯原子能形成氯化氢分子,而氢原子和氦原子在同一条件下却不能化合
想一想: 分子原子离子,三种微粒间存在着必然的联系,原子在形成分子或离子过程中,一般都形成稳定结构,则原子可通过哪些途径成为具有稳定结构的微粒
这些微粒之间的相互作用力有何不同
【同步导学】一、评价要点:1、了解化学键的概念及常见种类
2、知道离子键及其形成,知道离子化合物的概念
3、了解什么是电子式
知道用电子式表示离子键以及离子化合物
二、方法指引:1、化学键:存在于物质中直接相邻的原子或离子之间的强烈的相互作用
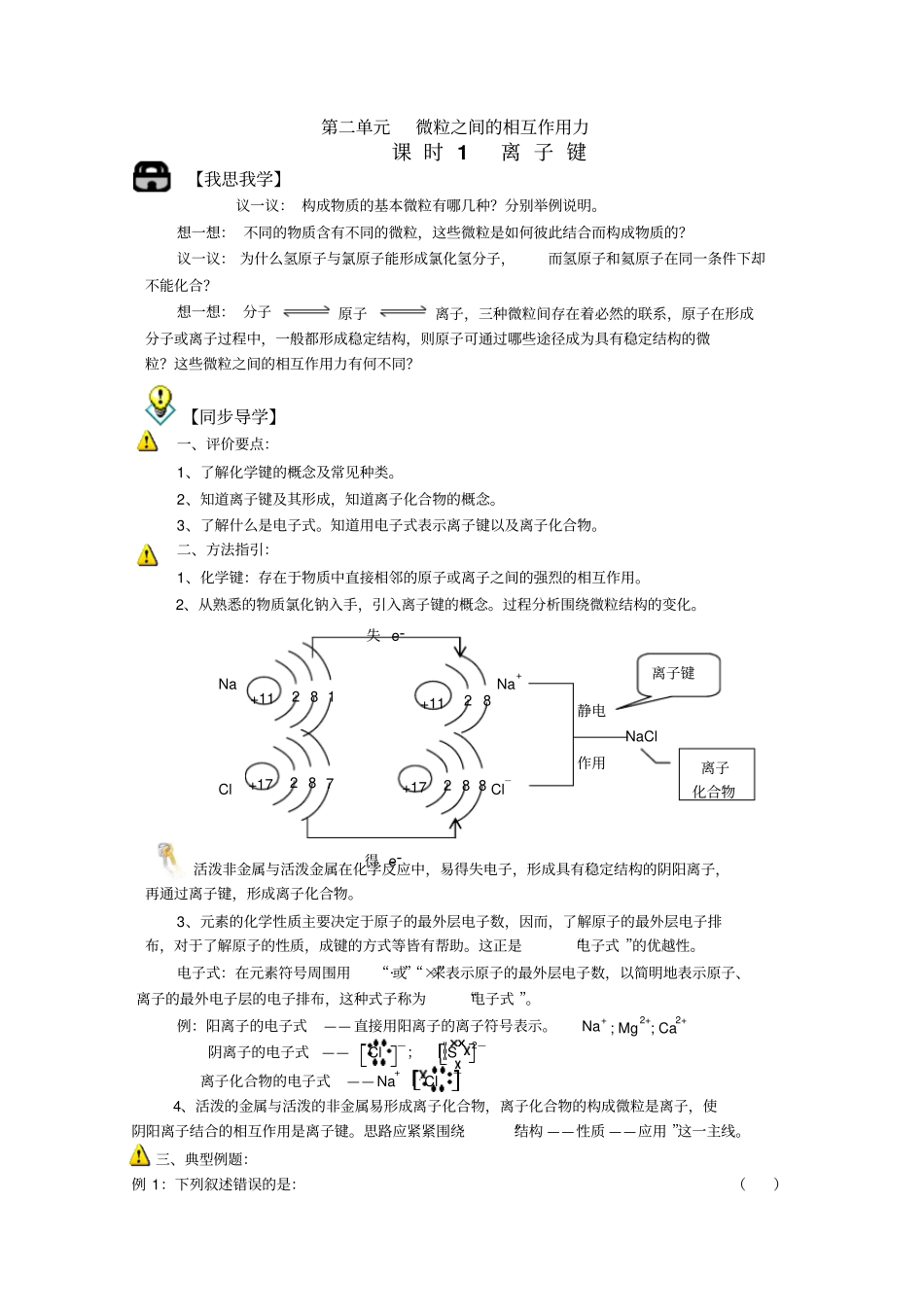
2、从熟悉的物质氯化钠入手,引入离子键的概念
过程分析围绕微粒结构的变化
Na Na+静电NaCl 作用Cl Cl—活泼非金属与活泼金属在化学反应中,易得失电子,形成具有稳定结构的阴阳离子,再通过离子键,形成离子化合物
3、元素的化学性质主要决定于原子的最外层电子数,因而,了解原子的最外层电子排布,对于了解原子的性质,成键的方式等皆有帮助
这正是“电子式 ”的优越性
电子式:在元素符号周围用“· ”或“×”来表示原子的最外层电子数,以简明地表示原子、离子的最外电子层的电子排布,这种式子称为“电子式 ”
例:阳离子的电子式—— 直接用阳离子的离子符号表示
Na+ ; Mg2+; Ca2+ 阴离子的电子式——Cl —;S 2—离子化合物的电子式—— Na+Cl —4、活泼的金属与活泼的非金属易形成离子化合物,离子化合物的构成微粒是离子,使阴阳离子结合的相互作用是离子键
思路应紧紧围绕“结构 ——性质 ——应用 ”这一主线
三、典型例题:例 1:下列叙述错误的是:()+11 8 2 +11 8 2