1 电 子 与原 子 碰 撞 实 验 实 验 2
1 弗 兰 克 ——赫兹实 验 引言 1913年,丹麦物理学家玻尔(N.Bohr)在卢瑟福原子核式模型的基础上,结合普朗克的量子理论,成功地解释了原子的稳定性和原子的线状光谱理论,玻尔理论是原子物理学发展史上的一个重要里程碑
在玻尔原子结构理论发表的第二年,即1914年,夫兰克(J.Frank)和赫兹(G.Hertz)用慢电子与稀薄气体原子碰撞的方法,使原子从低能级激发到较高能级
通过测量电子和原子碰撞时交换某一定值的能量,直接证明了原子内部量子化能级的存在,证明了原子发生跃迁时吸收和发射的能量是完全确定的,不连续的,给玻尔的原子理论提供了直接的而且是独立于光谱研究方法的实验证据
由于此项卓越的成就,他俩获得了1925年的诺贝尔物理学奖
实验目的 1
通过测定氩原子的第一激发电位,证明原子能级的存在
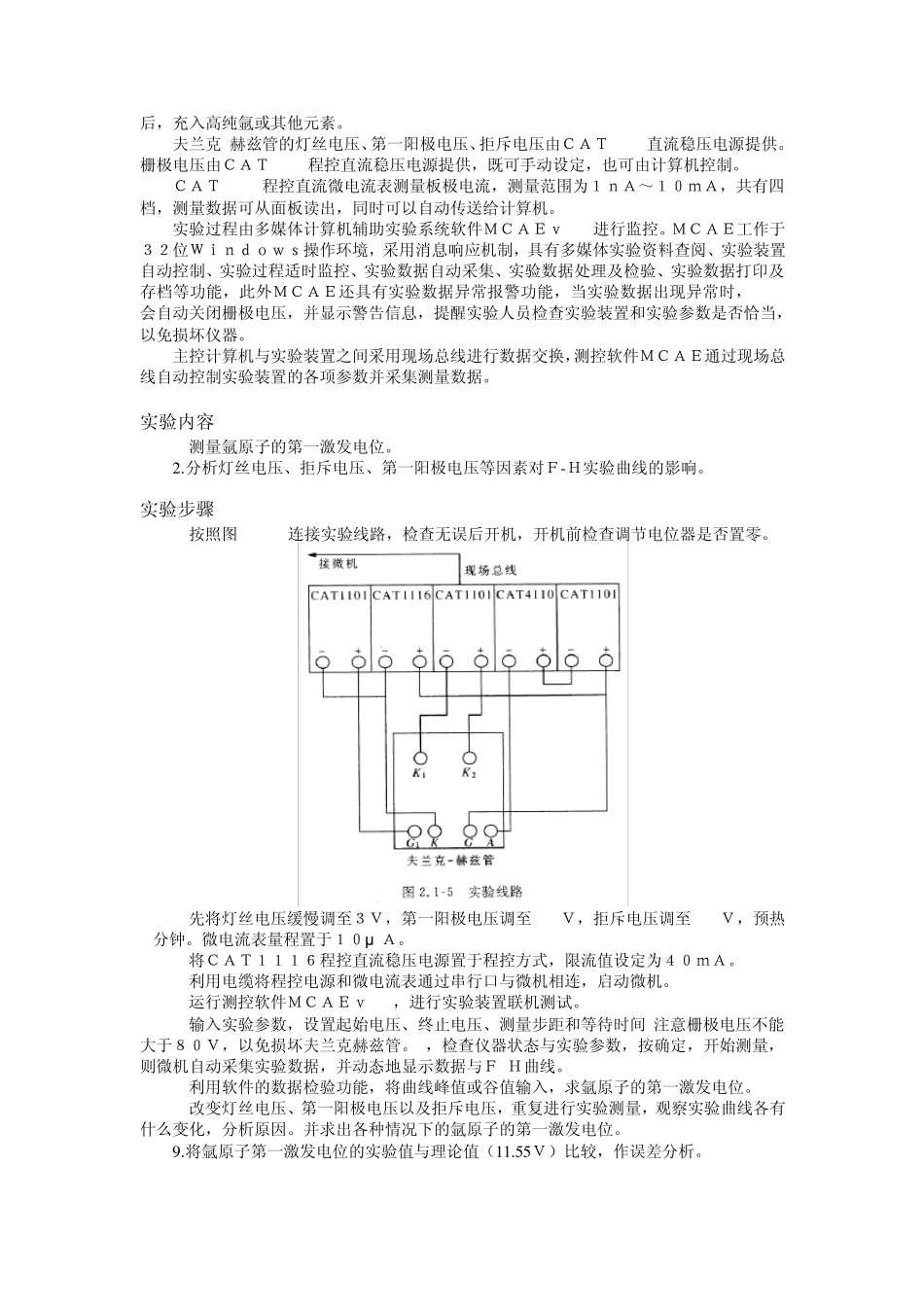
分析灯丝电压、拒斥电压等因素对F-H实验曲线的影响
了解计算机实时测控系统的一般原理和使用方法
实验原理 根据玻尔理论,原子只能较长久地停留在一些稳定状态(即定态),其中每一状态对应于一定的能量值,各定态的能量是分立的,原子只能吸收或辐射相当于两定态间能量差的能量
如果处于基态的原子要发生状态改变,所具备的能量不能少于原子从基态跃迁到第一激发态时所需要的能量
夫兰克-赫兹实验是通过具有一定能量的电子与原子碰撞,进行能量交换而实现原子从基态到高能态的跃迁
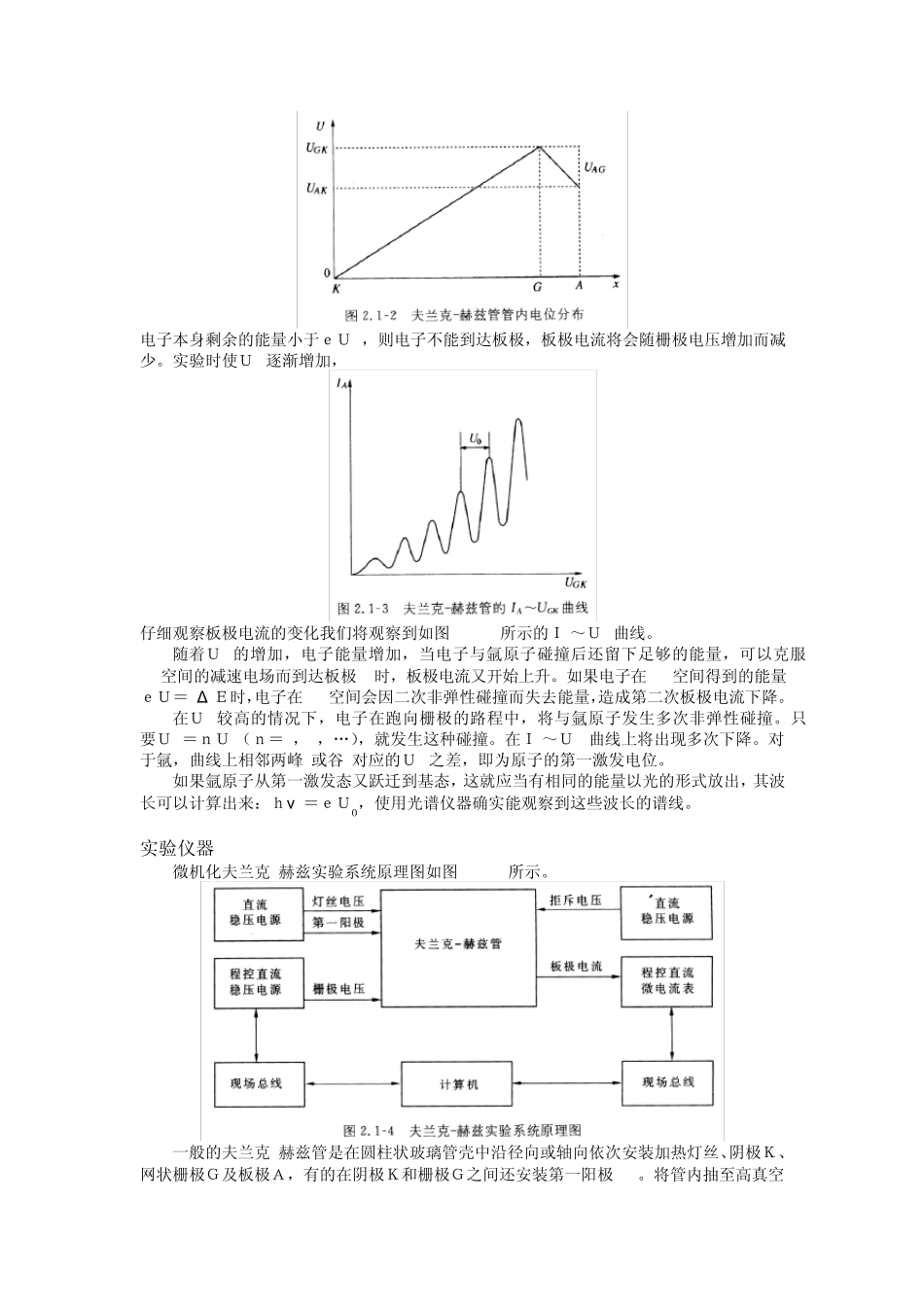
设氩原子的基态能量为E1,第一激发态的能量为E2,初速为零的电子在电位差为U0的加速电场作用下,获得能量为eU0,具有这种能量的电子与氩原子发生碰撞,当电子能量eU0<E2-E1时,电子与氩原子只能发生弹性碰撞,由于电子质量比氩原子质量小得多,电子能量损失很少
如果eU0≥E2-E1=Δ E,则电子与氩原子会产生非弹性碰撞
氩原子从电子中取得能