第 1 页 共 10 页 一
苯的结构与性质 1、苯的结构 (1)苯结构平面正六边形结构 碳碳键介于单键与双键间一种特殊键
对称性六个碳原子等效,六个氢原子等效
(2)苯的同系物是含有一个苯环和烷烃基(最多 6个)所形成的的化合物(3)芳香烃和芳香族:芳香烃是分子中含有一个或多个苯环的烃
而芳香族是分子中含有含有一个或多个苯环的化合物,芳香烃属于芳香族
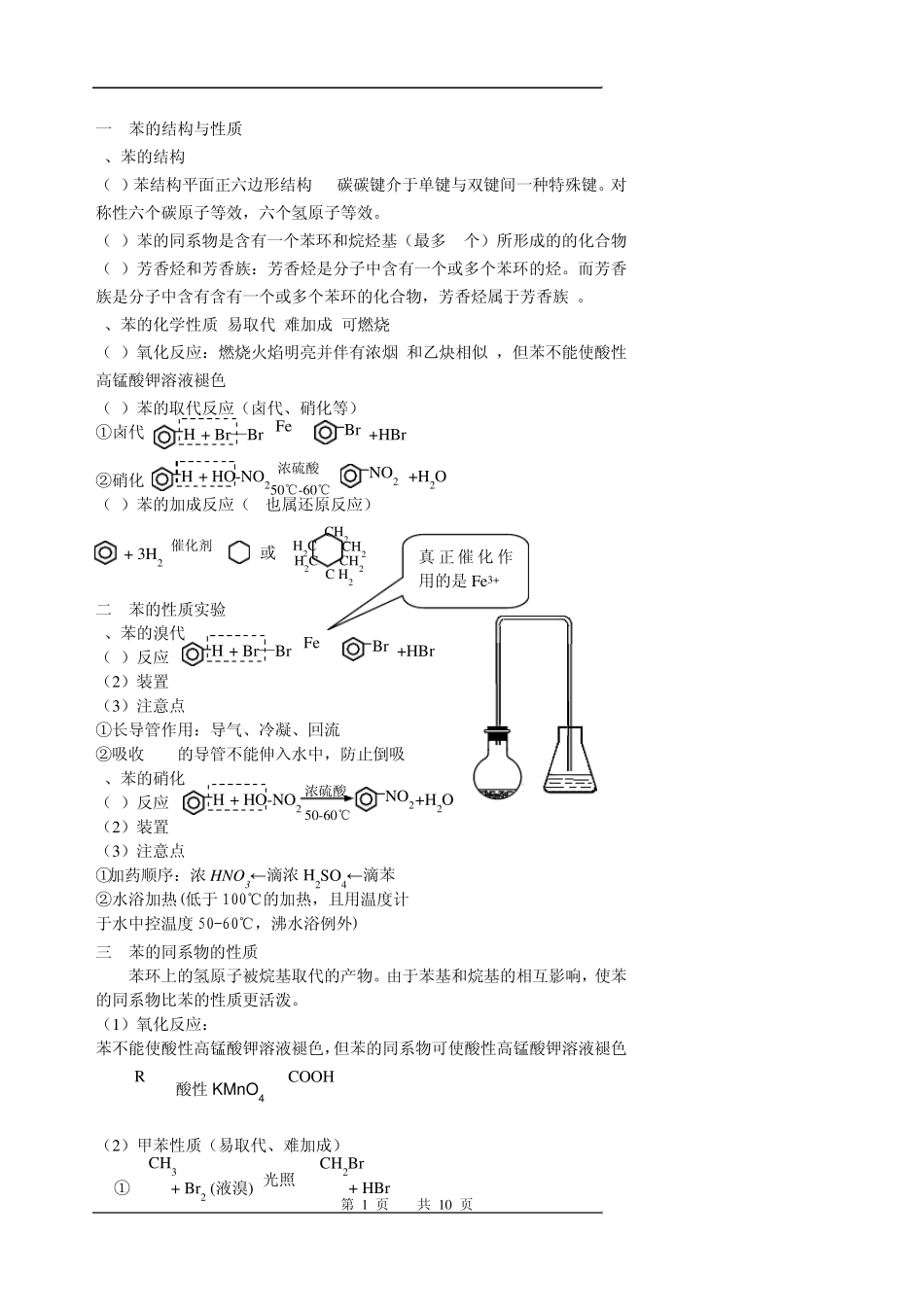
2、苯的化学性质 易取代 难加成 可燃烧 (1)氧化反应:燃烧火焰明亮并伴有浓烟(和乙炔相似),但苯不能使酸性高锰酸钾溶液褪色 (2)苯的取代反应(卤代、硝化等) ①卤代 ②硝化 (2)苯的加成反应(H2也属还原反应) 二
苯的性质实验 1、苯的溴代 (1)反应 (2)装置 (3)注意点 ①长导管作用:导气、冷凝、回流 ②吸收HBr的导管不能伸入水中,防止倒吸 2、苯的硝化 (1)反应 (2)装置 (3)注意点 ①加药顺序:浓 HNO3←滴浓 H2SO4←滴苯 ②水浴加热(低于 100℃的加热,且用温度计 于水中控温度50-60℃,沸水浴例外) 三
苯的同系物的性质 苯环上的氢原子被烷基取代的产物
由于苯基和烷基的相互影响,使苯的同系物比苯的性质更活泼
(1)氧化反应: 苯不能使酸性高锰酸钾溶液褪色,但苯的同系物可使酸性高锰酸钾溶液褪色 (2)甲苯性质(易取代、难加成) + Br—Br +HBr Br H Fe + 3H2 催化剂 CH2 C H2 CH2 CH2 H2C H2C 或 酸性 KMnO4 R COOH + HO-NO2 +H2O NO2 H 浓硫酸 50℃-60℃ 光照 + HBr CH3 ① + Br2 (液溴) CH2Br + Br—Br +HBr Br H Fe + HO-NO2 +H2O NO2 H 浓硫酸 50-60℃ 真 正 催 化 作用的是 Fe3+ 第 2 页 共 10 页 四