关于印发《药品 GMP 认证检查评定标准》的通知国食药监安[2024]648 号各省、自治区、直辖市食品药品监督管理局(药品监督管理局): 为进一步加强药品生产监督管理,切实做好药品 GMP 认证工作,全面提高认证工作质量,国家局对《药品 GMP 认证检查评定标准(试行)》进行了修订
现将修订后的《药品 GMP 认证检查评定标准》印发给你们,该标准自 2024 年 1 月 1 日起施行
国家食品药品监督管理局 二○○七年十月二十四日药品 GMP 认证检查评定标准一、药品 GMP 认证检查项目共 259 项,其中关键项目(条款号前加“*”)92 项,一般项目 167 项
二、药品 GMP 认证检查时,应根据申请认证的范围确定相应的检查项目,并进行全面检查和评定
三、检查中发现不符合要求的项目统称为“缺陷项目”
其中,关键项目不符合要求者称为“严重缺陷”,一般项目不符合要求者称为“一般缺陷”
四、缺陷项目假如在申请认证的各剂型或产品中均存在,应按剂型或产品分别计算
五、在检查过程中,企业隐瞒有关情况或提供虚假材料的,按严重缺陷处理
检查组应调查取证并详细记录
六、结果评定(一)未发现严重缺陷,且一般缺陷≤20%,能够立即改正的,企业必须立即改正;不能立即改正的,企业必须提供缺陷整改报告及整改计划,方可通过药品 GMP 认证
(二)严重缺陷或一般缺陷>20%的,不予通过药品 GMP 认证
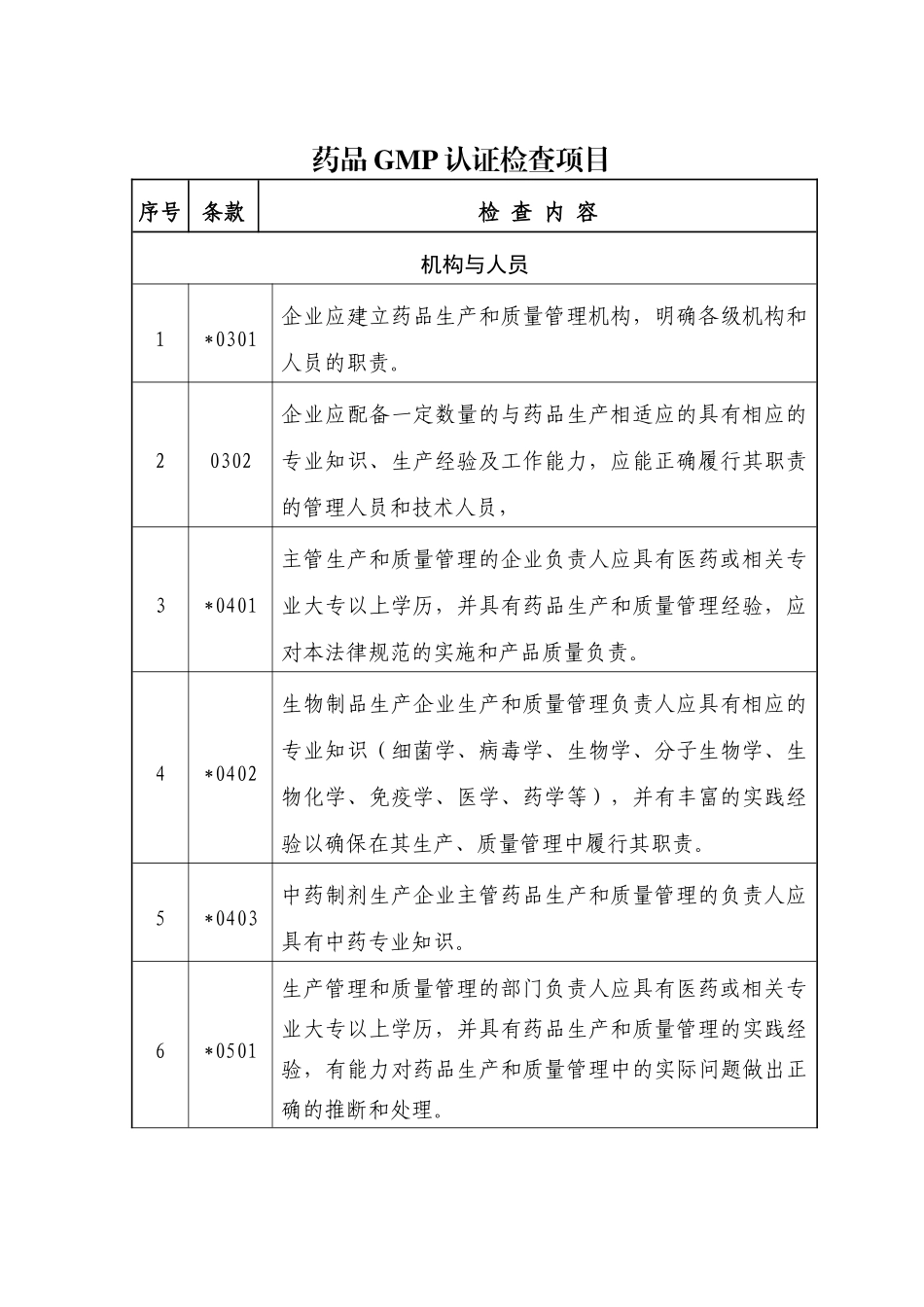
药品 GMP 认证检查项目序号条款检 查 内 容机构与人员1*0301企业应建立药品生产和质量管理机构,明确各级机构和人员的职责
20302企业应配备一定数量的与药品生产相适应的具有相应的专业知识、生产经验及工作能力,应能正确履行其职责的管理人员和技术人员, 3*0401主管生产和质量管理的企业负责人应具有医药或相关专业大专以上学历,并具有药品生产和质量管理经验,应对本法律规范的实施和产品质量