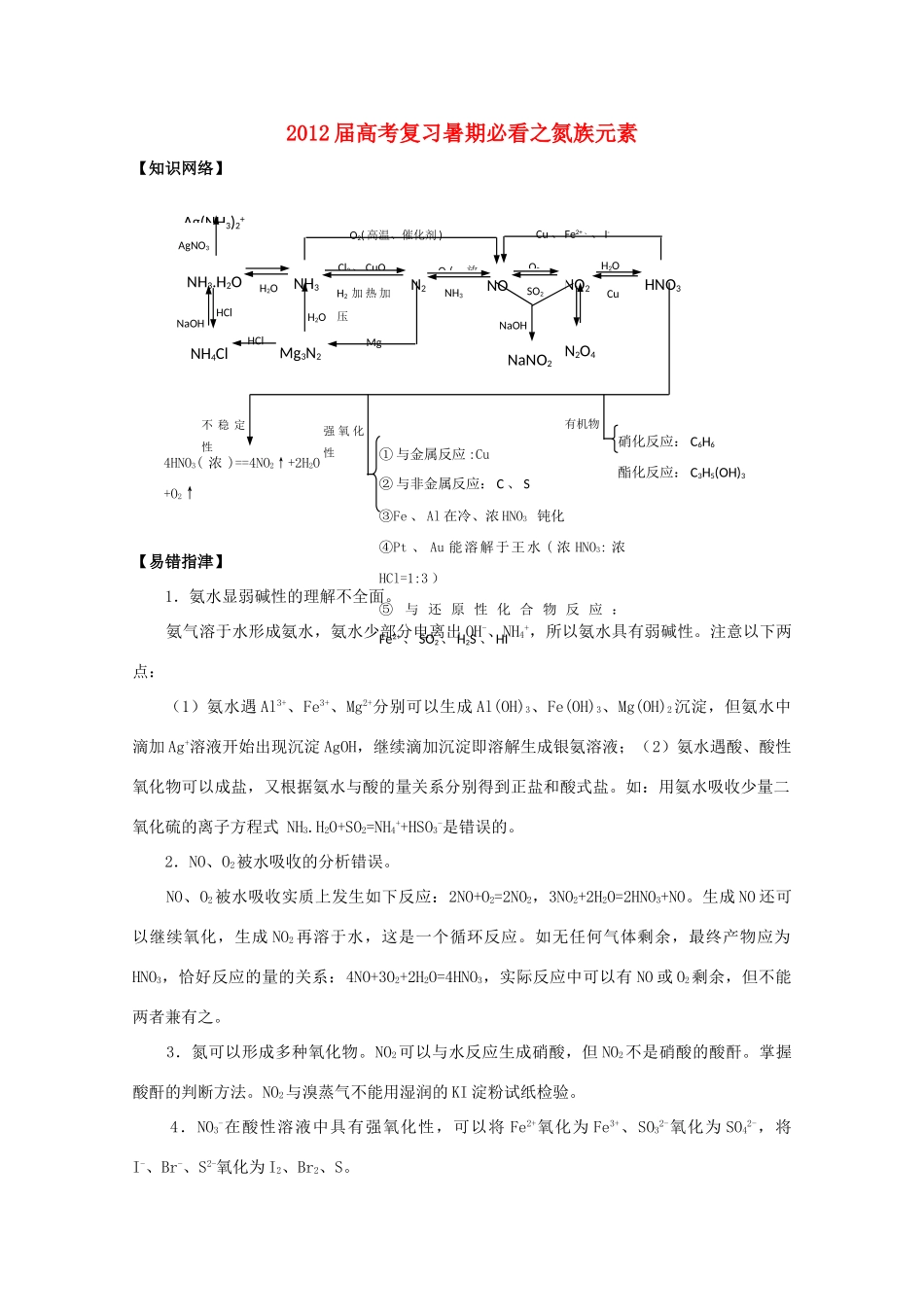
2012 届高考复习暑期必看之氮族元素【知识网络】【易错指津】 1.氨水显弱碱性的理解不全面
氨气溶于水形成氨水,氨水少部分电离出 OH-、NH4+,所以氨水具有弱碱性
注意以下两点:(1)氨水遇 Al3+、Fe3+、Mg2+分别可以生成 Al(OH)3、Fe(OH)3、Mg(OH)2沉淀,但氨水中滴加 Ag+溶液开始出现沉淀 AgOH,继续滴加沉淀即溶解生成银氨溶液;(2)氨水遇酸、酸性氧化物可以成盐,又根据氨水与酸的量关系分别得到正盐和酸式盐
如:用氨水吸收少量二氧化硫的离子方程式 NH3
H2O+SO2=NH4++HSO3-是错误的
2.NO、O2被水吸收的分析错误
NO、O2被水吸收实质上发生如下反应:2NO+O2=2NO2,3NO2+2H2O=2HNO3+NO
生成 NO 还可以继续氧化,生成 NO2 再溶于水,这是一个循环反应
如无任何气体剩余,最终产物应为HNO3,恰好反应的量的关系:4NO+3O2+2H2O=4HNO3,实际反应中可以有 NO 或 O2剩余,但不能两者兼有之
3.氮可以形成多种氧化物
NO2可以与水反应生成硝酸,但 NO2不是硝酸的酸酐
掌握酸酐的判断方法
NO2与溴蒸气不能用湿润的 KI 淀粉试纸检验
4.NO3-在酸性溶液中具有强氧化性,可以将 Fe2+氧化为 Fe3+、SO32-氧化为 SO42-,将I-、Br-、S2-氧化为 I2、Br2、S
O2( 高温、催化剂 )4HNO3( 浓 )==4NO2↑+2H2O+O2↑强 氧 化性不 稳 定性HNO3NaNO2NaOHMgN2O4H2ONH3
H2ONH3N2NONO2Ag(NH3)2+NH4ClAgNO3NaOHHClΔH2OMg3N2Cl2、 CuOH2 加 热 加压O2(放电 )NH3O2SO2H2OCuHClCu 、 Fe2+ 、、 I-① 与金属反应 :Cu② 与非