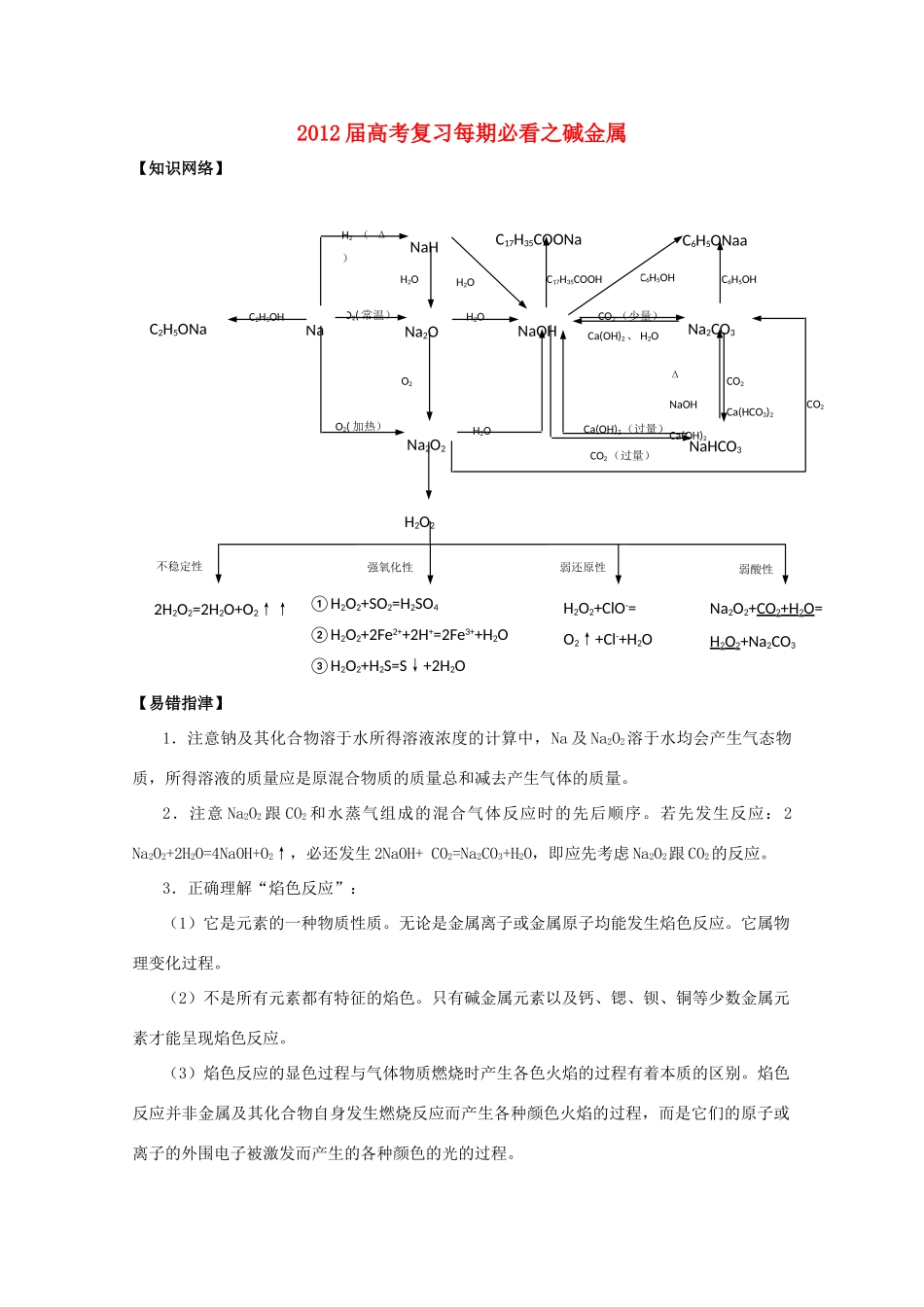
2012 届高考复习每期必看之碱金属【知识网络】【易错指津】1.注意钠及其化合物溶于水所得溶液浓度的计算中,Na 及 Na2O2溶于水均会产生气态物质,所得溶液的质量应是原混合物质的质量总和减去产生气体的质量
2.注意 Na2O2 跟 CO2 和水蒸气组成的混合气体反应时的先后顺序
若先发生反应:2 Na2O2+2H2O=4NaOH+O2↑,必还发生 2NaOH+ CO2=Na2CO3+H2O,即应先考虑 Na2O2跟 CO2的反应
3.正确理解“焰色反应”:(1)它是元素的一种物质性质
无论是金属离子或金属原子均能发生焰色反应
它属物理变化过程
(2)不是所有元素都有特征的焰色
只有碱金属元素以及钙、锶、钡、铜等少数金属元素才能呈现焰色反应
(3)焰色反应的显色过程与气体物质燃烧时产生各色火焰的过程有着本质的区别
焰色反应并非金属及其化合物自身发生燃烧反应而产生各种颜色火焰的过程,而是它们的原子或离子的外围电子被激发而产生的各种颜色的光的过程
Ca(OH)2、 H2OC6H5OHCO2CO2(过量)Ca(OH)2(过量)H2OC17H35COOHH2OH2ONa2CO3NaHCO3ΔNaOHCa(OH)2CO2Ca(HCO3)2O2O2( 常温)NaNa2ONa2O2NaOHC6H5ONaaH2OCO2(少量)C6H5OHO2( 加热)NaHC17H35COONaH2 ( Δ)C2H5ONaC2H5OH不稳定性H2O2强氧化性弱还原性弱酸性2H2O2=2H2O+O2↑↑①H2O2+SO2=H2SO4②H2O2+2Fe2++2H+=2Fe3++H2O③H2O2+H2S=S↓+2H2OH2O2+ClO-=O2↑+Cl-+H2ONa2O2+CO2+H2O= H2O2+Na2CO3【典型例题评析】例 1 碱金属与卤素所形成的化合物大都具有的性质是、① 高沸点 ②能溶于水 ③水溶液