2014 年高中化学《金属及其化合物》全章复习与巩固基础知识讲解导学案 新人教版必修 1【学习目标】1、了解钠、铝、铁、铜等金属及其重要化合物的主要性质;2、通过金属及其化合物性质的实验,培养实验意识、操作技能、观察能力和分析问题的能力;3、以金属知识的学习为线索,培养获取知识及信息加工的能力
通过比较、归纳等,逐步掌握学习元素化合物的一般方法
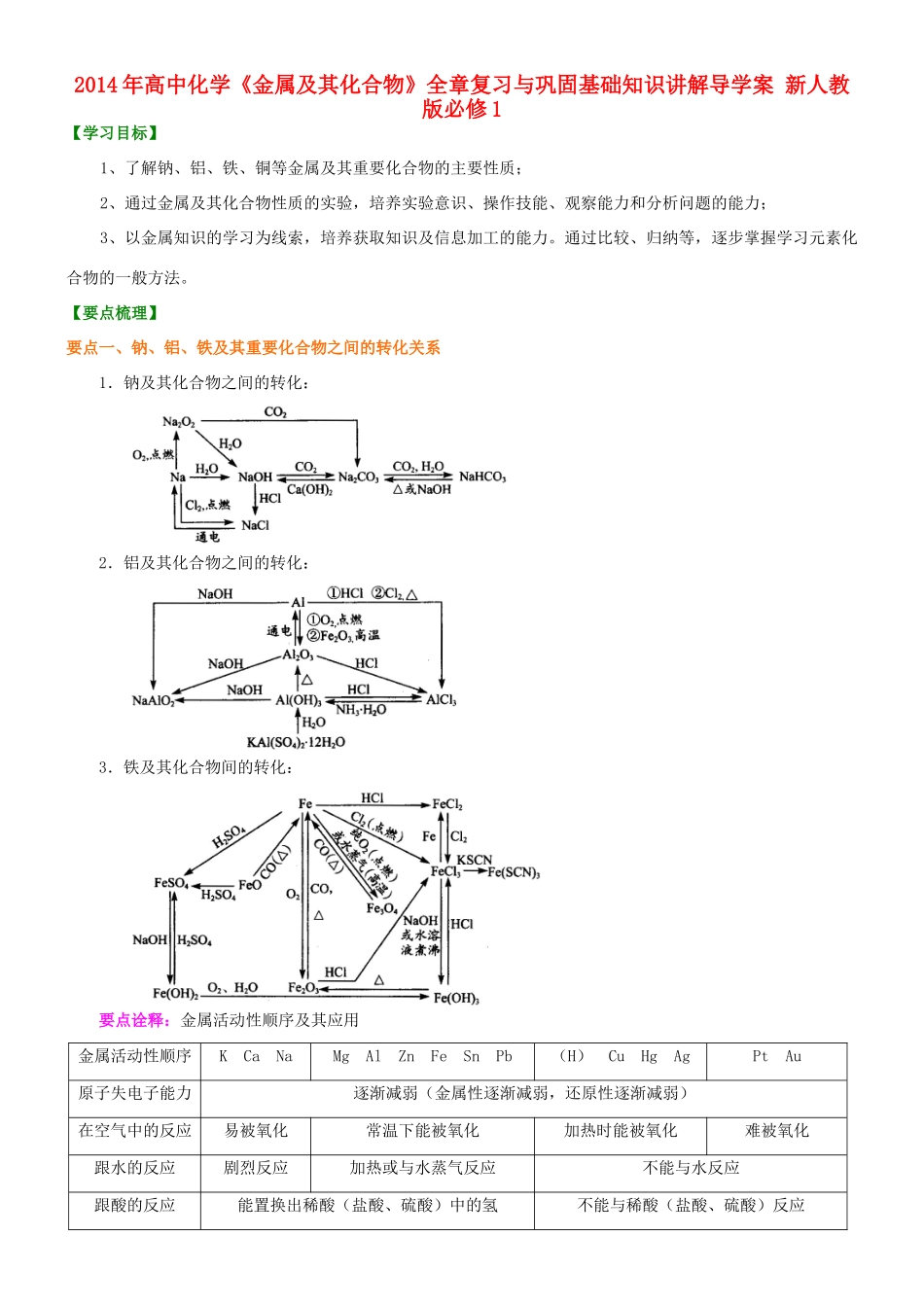
【要点梳理】要点一、钠、铝、铁及其重要化合物之间的转化关系 1.钠及其化合物之间的转化: 2.铝及其化合物之间的转化: 3.铁及其化合物间的转化: 要点诠释:金属活动性顺序及其应用金属活动性顺序K Ca NaMg Al Zn Fe Sn Pb(H) Cu Hg AgPt Au原子失电子能力逐渐减弱(金属性逐渐减弱,还原性逐渐减弱)在空气中的反应易被氧化常温下能被氧化加热时能被氧化难被氧化跟水的反应剧烈反应加热或与水蒸气反应不能与水反应跟酸的反应能置换出稀酸(盐酸、硫酸)中的氢不能与稀酸(盐酸、硫酸)反应剧烈反应反应剧烈程度减弱跟硝酸、浓硫酸反应溶于王水跟盐溶液的反应与水先反应金属活动性顺序表中前面的金属能将后面的金属从其盐溶液中置换出来跟强碱溶液反应Al、Zn 等金属能跟强碱溶液发生反应要点二、碳酸钠和碳酸氢钠的关系总结 1.俗名:Na2CO3:纯碱、苏打;NaHCO3:小苏打
2.溶解度:Na2CO3>NaHCO3
3.热稳定性:Na2CO3>NaHCO3(一般温度下 Na2CO3不分解)
4.其固体跟同浓度的盐酸反应产生气体的速率:Na2CO3<NaHCO3
5.将稀盐酸逐滴加入到 Na2CO3、NaHCO3的水溶液中,发生的反应与现象分别为: Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=CO2↑+H2O+NaCl
现象:开始无气体产生,盐酸滴加一定量后(Na2CO3全部转化为 NaHCO3),