第 2 节 化学反应的限度第 1 课时 化学平衡常数[学习目标定位] 1
知道化学平衡常数的含义,会根据化学反应书写化学平衡常数表达式,知道化学平衡常数的影响因素
能根据化学平衡常数表示的意义,判断反应进行的程度和方向
1.化学平衡状态的概念:如果外界条件(温度、浓度、压强等)不发生改变,当可逆反应进行到一定程度时,正反应速率与逆反应速率相等,反应物的浓度与生成物的浓度不再改变,达到一种表面静止的状态,称为“化学平衡状态”,简称化学平衡
化学平衡研究的对象是可逆反应
2.化学平衡状态的特征:(1)等:v 正=v 逆≠0
(2)动:化学平衡状态是一种动态平衡
达到平衡状态时,反应并没有停止,这时正反应和逆反应都依然在进行
(3)定:反应物的浓度和生成物的浓度不再改变
(4)变:外界条件(温度、浓度、压强等)一旦改变,化学平衡状态就会被破坏,并在新的条件下建立新的化学平衡
3.一定温度下,在 10 L 密闭容器中加入 5 mol SO2和 3 mol O2,当反应达到平衡时,有 3 mol SO2发生了反应,则:(1)生成了________mol SO3
(2)平衡时容器内气体的总物质的量为________
(3)平衡时 SO2的浓度是__________,O2的浓度是________________________________,SO3的浓度是__________
答案 (1)3 (2)6
5 mol (3)0
2 mol·L-10.15 mol·L-1 0
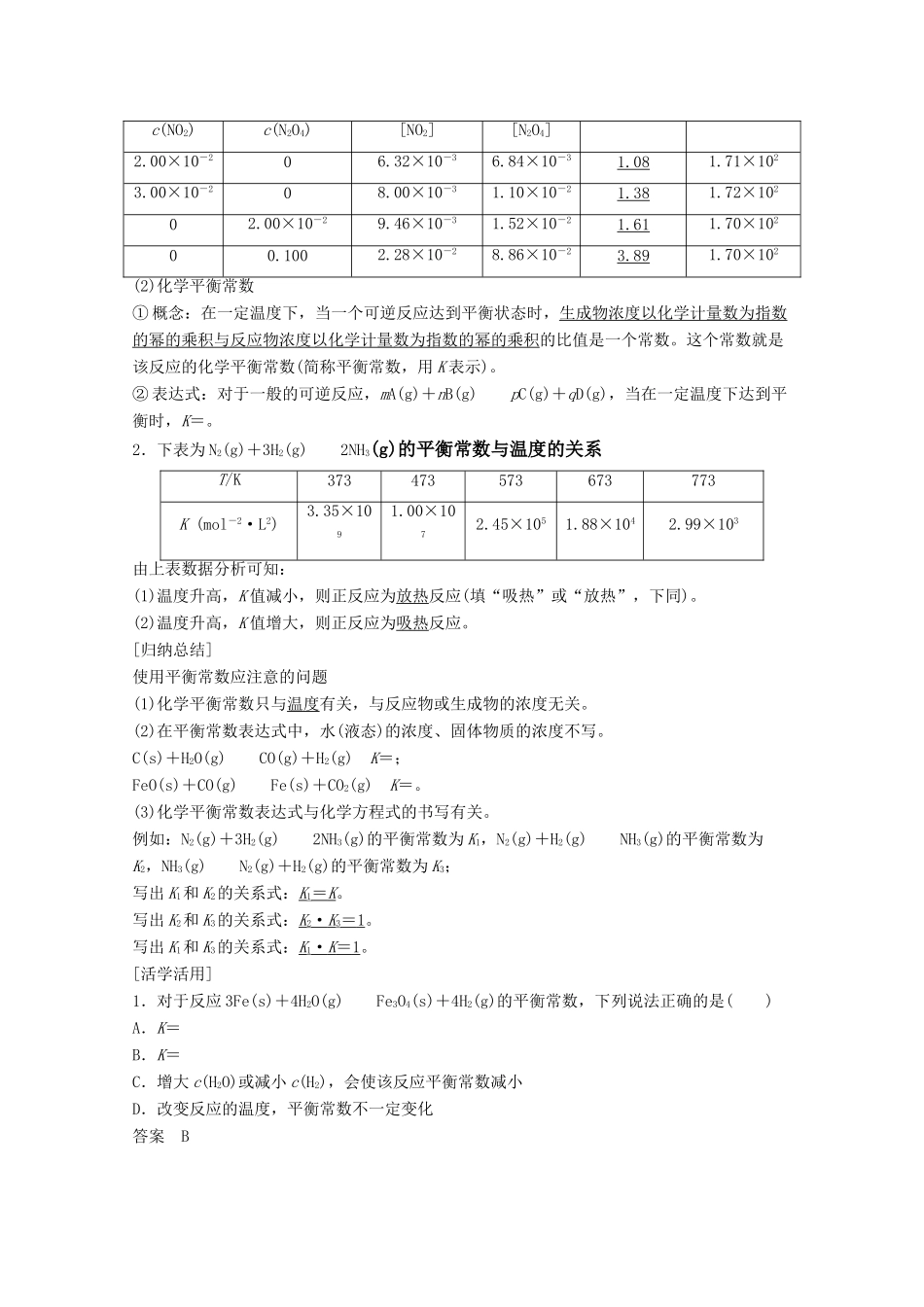
3 mol·L-1探究点一 化学平衡常数的概念及其表达式1.二氧化氮、四氧化二氮的相互转化是一个可逆反应:2NO2(g)N2O4(g),在 298 K,如果用不同起始浓度的二氧化氮或四氧化二氮进行反应,平衡后得到以下实验数据
(1)请根据表中已知数据填写空格:起始浓度/mol·L-1平衡浓度/mol·L-1平衡