第三节 常见气体的制备 实验设计与评价考纲点击1.了解化学实验是科学探究过程中的一种重要方法
2.掌握常见气体的实验室制法(包括所用试剂、仪器,反应原理和收集方法)
3.能根据实验试题要求,做到:①设计、评价或改进实验方案;②了解控制实验条件的方法;③分析或处理实验数据,得出合理结论;④绘制和识别典型的实验仪器装置图
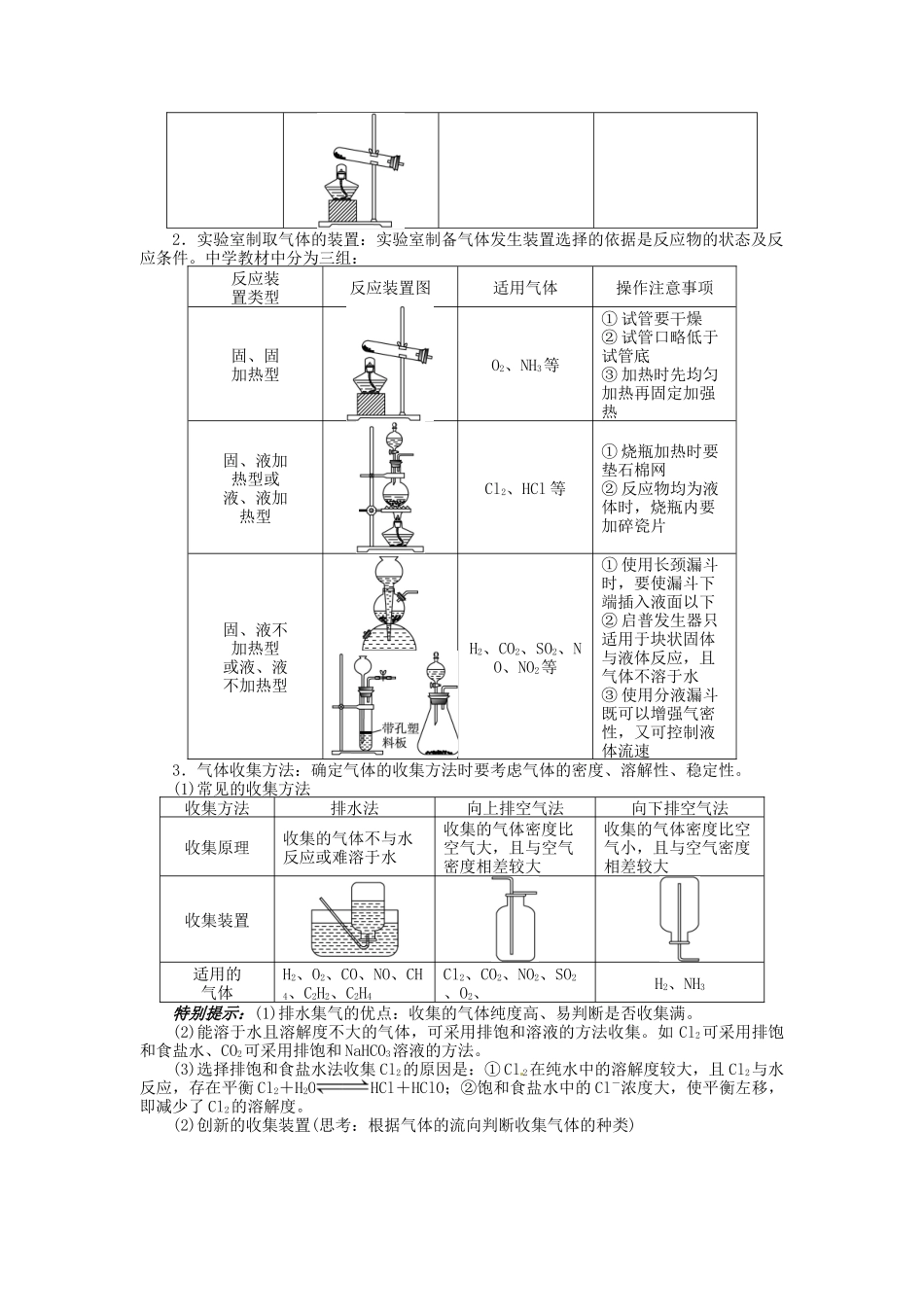
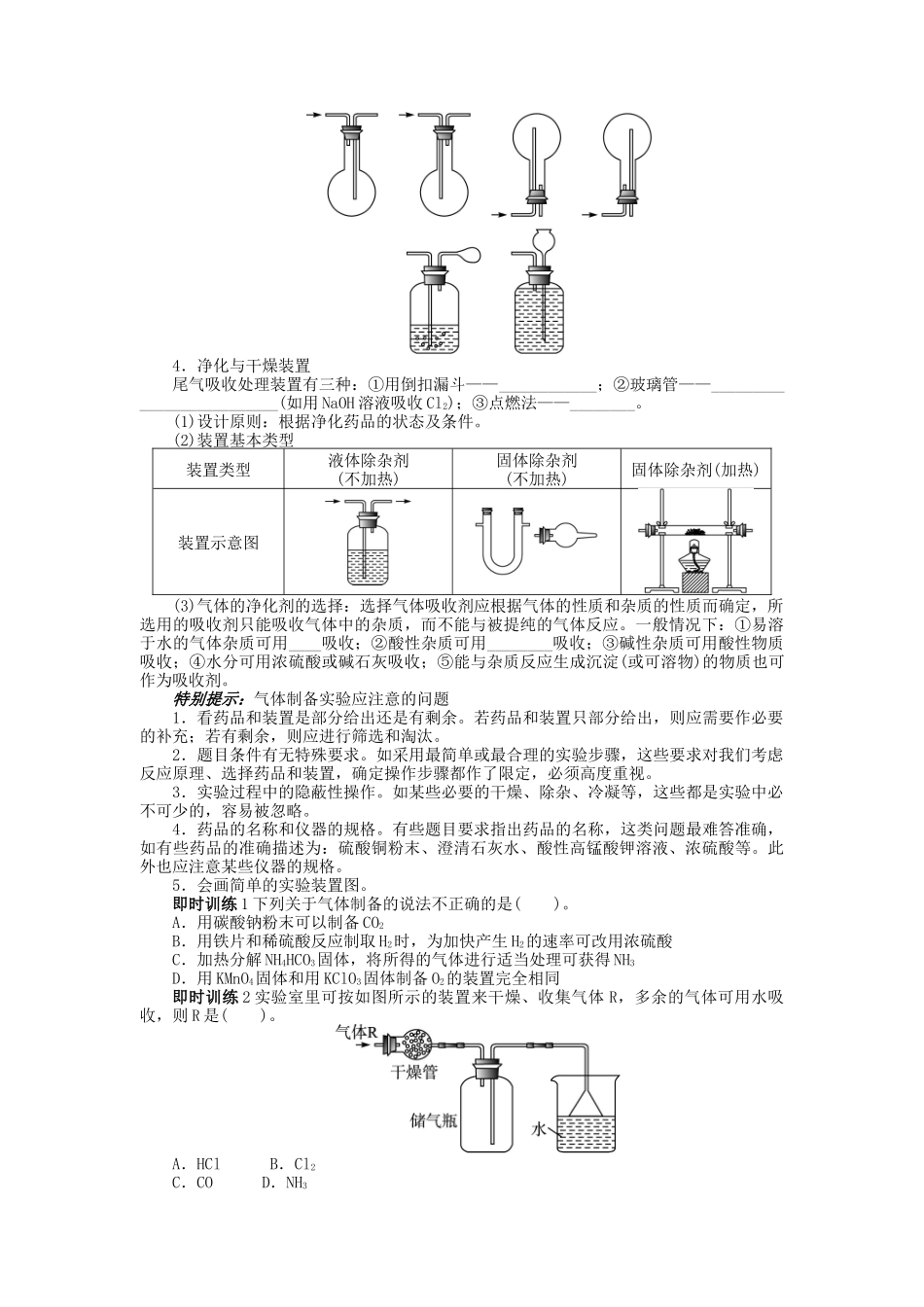
一、常见气体的制备、收集、干燥与净化1.常见气体的实验室制备制取装置反应原理收集方法氧气二氧化碳氢气氯气氨气2.实验室制取气体的装置:实验室制备气体发生装置选择的依据是反应物的状态及反应条件
中学教材中分为三组:反应装置类型反应装置图适用气体操作注意事项固、固加热型O2、NH3等① 试管要干燥② 试管口略低于试管底③ 加热时先均匀加热再固定加强热固、液加热型或液、液加热型Cl2、HCl 等① 烧瓶加热时要垫石棉网② 反应物均为液体时,烧瓶内要加碎瓷片固、液不加热型或液、液不加热型H2、CO2、SO2、NO、NO2等① 使用长颈漏斗时,要使漏斗下端插入液面以下② 启普发生器只适用于块状固体与液体反应,且气体不溶于水③ 使用分液漏斗既可以增强气密性,又可控制液体流速3.气体收集方法:确定气体的收集方法时要考虑气体的密度、溶解性、稳定性
(1)常见的收集方法收集方法排水法向上排空气法向下排空气法收集原理收集的气体不与水反应或难溶于水收集的气体密度比空气大,且与空气密度相差较大收集的气体密度比空气小,且与空气密度相差较大收集装置适用的气体H2、O2、CO、NO、CH4、C2H2、C2H4Cl2、CO2、NO2、SO2、O2、H2、NH3特别提示:(1)排水集气的优点:收集的气体纯度高、易判断是否收集满
(2)能溶于水且溶解度不大的气体,可采用排饱和溶液的方法收集
如 Cl2可采用排饱和食盐水、CO2可采用排饱和 NaHCO3溶液的方法
(3)选择排饱和食盐水法收集 C