第 1 节 化学反应的热效应课标解读要点网络1
了解化学反应中能量转化的原因及常见的能量转化形式
2.了解化学能与热能的相互转化
了解吸热反应、放热反应、反应热等概念
3.了解热化学方程式的含义,能正确书写热化学方程式
4.了解能源是人类生存和社会发展的重要基础
了解化学在解决能源危机中的重要作用
5.了解焓变(ΔH)与反应热的含义
了解活化能的概念
6.理解盖斯定律,并能运用盖斯定律进行有关反应焓变的计算
焓变 热化学方程式1.化学反应中的能量变化(1)化学反应中的两大变化:物质变化和能量变化
(2)化学反应中的两大守恒:质量守恒和能量守恒
(3)化学反应中的能量转化形式① 吸热反应:热能―→化学能
② 放热反应:化学能―→热能
③ 光合作用:光能―→化学能
④ 燃烧反应:化学能―→热能,化学能―→光能
⑤ 原电池反应:化学能―→电能
⑥ 电解池反应:电能―→化学能
(4)化学反应的实质与特征2.焓变、反应热(1)焓(H)用于描述物质所具有能量的物理量
(2)焓变(ΔH)ΔH=H ( 生成物 ) - H ( 反应物 )
单位 kJ·mol-1或 kJ/mol
(3)反应热指当化学反应在一定的温度下进行时,反应所释放或吸收的热量,通常用符号 Q 表示,单位 kJ·mol-1
(4)焓变与反应热的关系对于恒压条件下进行的化学反应,如果反应中物质的能量变化全部转化为热能,则有关系:Δ H = Q p
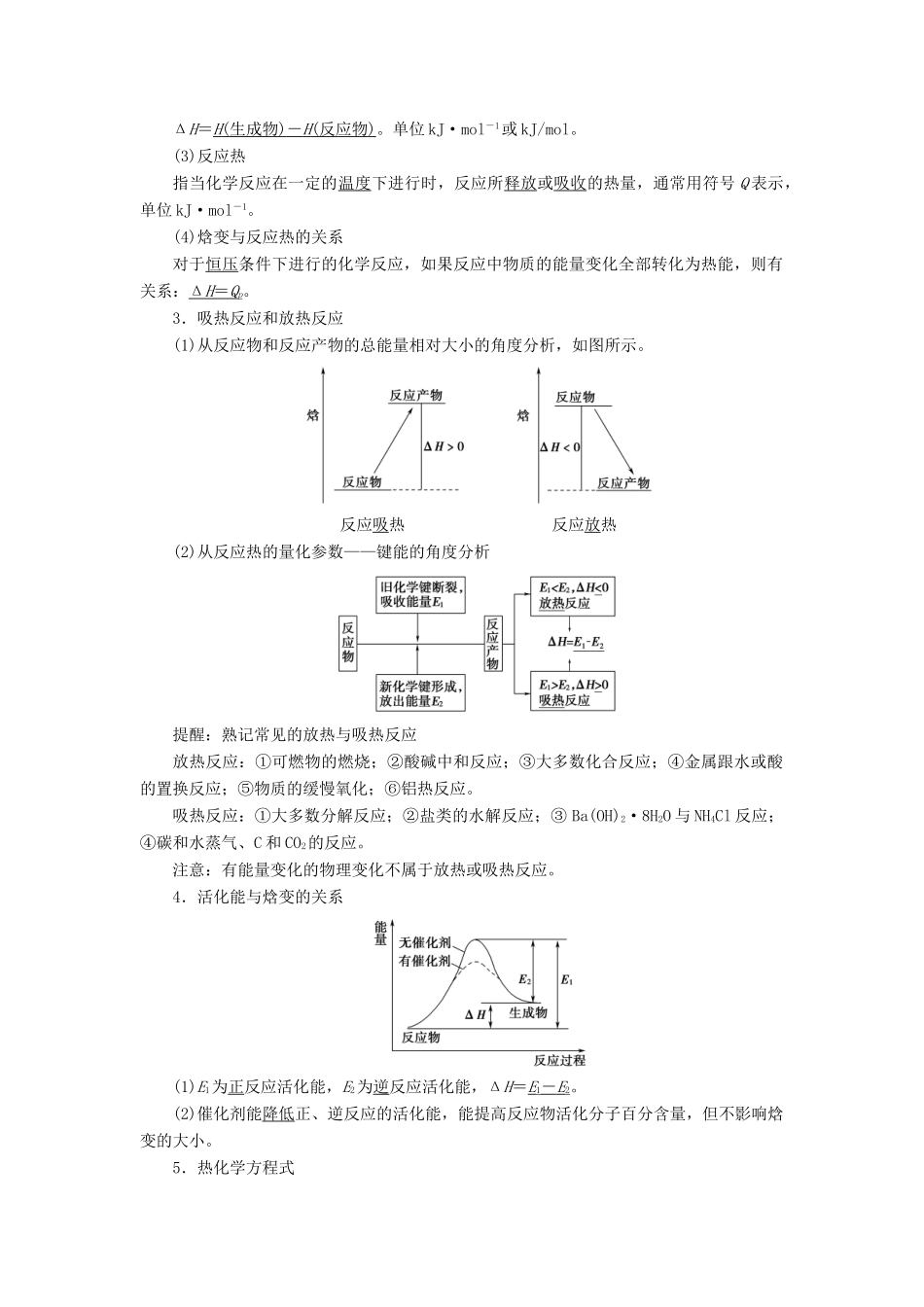
3.吸热反应和放热反应(1)从反应物和反应产物的总能量相对大小的角度分析,如图所示
反应吸热 反应放热(2)从反应热的量化参数——键能的角度分析提醒:熟记常见的放热与吸热反应放热反应:①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟水或酸的置换反应;⑤物质的缓慢氧化;⑥铝热反应
吸热反应:①大多数分解反应;②盐类的水解反应;③ Ba(OH)2·8H2O 与 NH4Cl