第一单元 铁、铜的获取及应用学习任务 1 铁及其重要化合物的性质一、铁元素及其原子结构1.铁位于周期表中第 4 周期Ⅷ族,是一种应用最广泛的过渡金属元素;铁元素是一种典型的变价金属元素
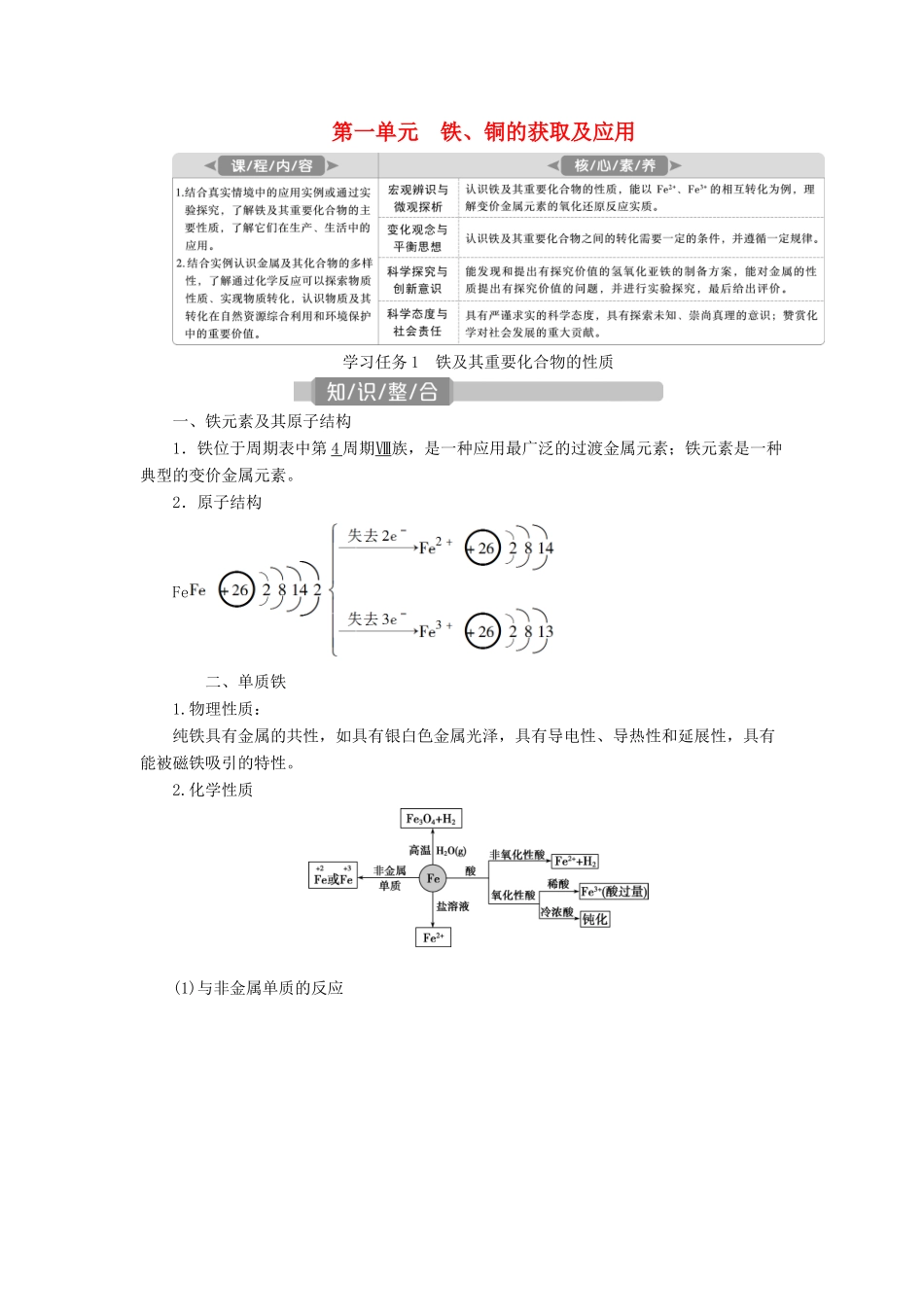
2.原子结构Fe 二、单质铁1
物理性质:纯铁具有金属的共性,如具有银白色金属光泽,具有导电性、导热性和延展性,具有能被磁铁吸引的特性
化学性质(1)与非金属单质的反应(2)与水蒸气的反应3Fe+4H2O(g)=====Fe3O4+4H2(3)与酸、盐的反应3.用途:用量最大、用途最广泛的合金是铁合金——钢,可用于制造不锈钢、特种钢、钢板、钢管等
三、铁的冶炼1.铁元素的存在铁元素在自然界主要以化合态的形式存在,常见的铁矿有磁铁矿(主要成分为 Fe3O4)、赤铁矿(主要成分为 Fe2O3)
2.炼铁原料:铁矿石、焦炭、空气、石灰石
3.完成下列化学方程式(1)一氧化碳的生成:C + O 2===== CO 2、 CO 2+ C ===== 2CO
(2)铁矿石被还原:Fe2O3+ 3CO ===== 2Fe + 3CO 2
(3)石灰石的作用:CaCO3===== CaO + CO 2↑ 、 CaO + SiO 2===== CaSiO 3
四、铁的氧化物化学式FeOFe2O3Fe3O4俗名—铁红磁性氧化铁颜色状态黑色粉末红棕色粉末黑色晶体(有磁性)溶解性难溶于水难溶于水难溶于水铁的化合价+2+3+ 2 , + 3 稳定性不稳定稳定稳定与盐酸反应的离子方程式FeO+2H+===Fe2++H2OFe2O3+ 6H + == =2Fe 3 + + 3H 2OFe3O4+8H+===Fe2++2Fe3++4H2O五、铁的氢氧化物化学式Fe(OH)2Fe(OH)3色态白色固体红褐色固体与盐酸反应的离子方程式Fe(OH)2+2H+===Fe2++2H2OFe(OH)3+3H+===Fe3++3H