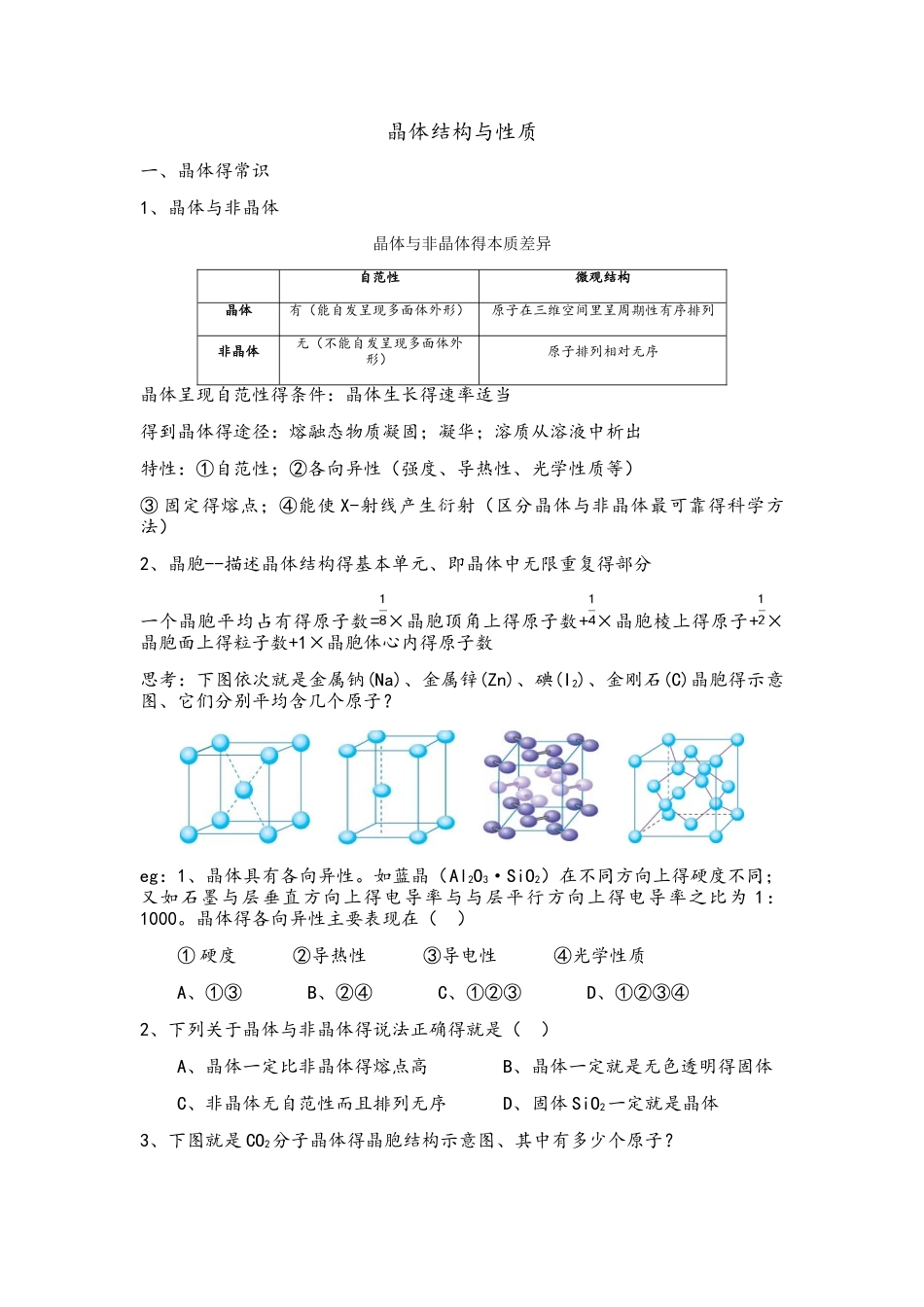
晶体结构与性质一、晶体得常识1、晶体与非晶体晶体与非晶体得本质差异自范性微观结构晶体有(能自发呈现多面体外形)原子在三维空间里呈周期性有序排列非晶体无(不能自发呈现多面体外形)原子排列相对无序晶体呈现自范性得条件:晶体生长得速率适当得到晶体得途径:熔融态物质凝固;凝华;溶质从溶液中析出特性:①自范性;②各向异性(强度、导热性、光学性质等)③ 固定得熔点;④能使 X-射线产生衍射(区分晶体与非晶体最可靠得科学方法)2、晶胞--描述晶体结构得基本单元、即晶体中无限重复得部分一个晶胞平均占有得原子数= ×晶胞顶角上得原子数+ ×晶胞棱上得原子+ ×晶胞面上得粒子数+1×晶胞体心内得原子数思考:下图依次就是金属钠(Na)、金属锌(Zn)、碘(I2)、金刚石(C)晶胞得示意图、它们分别平均含几个原子
eg:1、晶体具有各向异性
如蓝晶(Al2O3·SiO2)在不同方向上得硬度不同;又如石墨与层垂直方向上得电导率与与层平行方向上得电导率之比为 1:1000
晶体得各向异性主要表现在( )① 硬度 ②导热性 ③导电性 ④光学性质A、①③ B、②④ C、①②③ D、①②③④2、下列关于晶体与非晶体得说法正确得就是( )A、晶体一定比非晶体得熔点高 B、晶体一定就是无色透明得固体C、非晶体无自范性而且排列无序 D、固体 SiO2一定就是晶体3、下图就是 CO2分子晶体得晶胞结构示意图、其中有多少个原子
二、分子晶体与原子晶体1、分子晶体--分子间以分子间作用力(范德华力、氢键)相结合得晶体注意:a、构成分子晶体得粒子就是分子b、分子晶体中、分子内得原子间以共价键结合、相邻分子间以分子间作用力结合① 物理性质a、较低得熔、沸点 b、较小得硬度c、一般都就是绝缘体、熔融状态也不导电d、“相似相溶原理”:非极性分子一般能溶于非极性溶剂、极性分子一般能溶于极性溶剂② 典型得分子晶体a、非金属氢化物