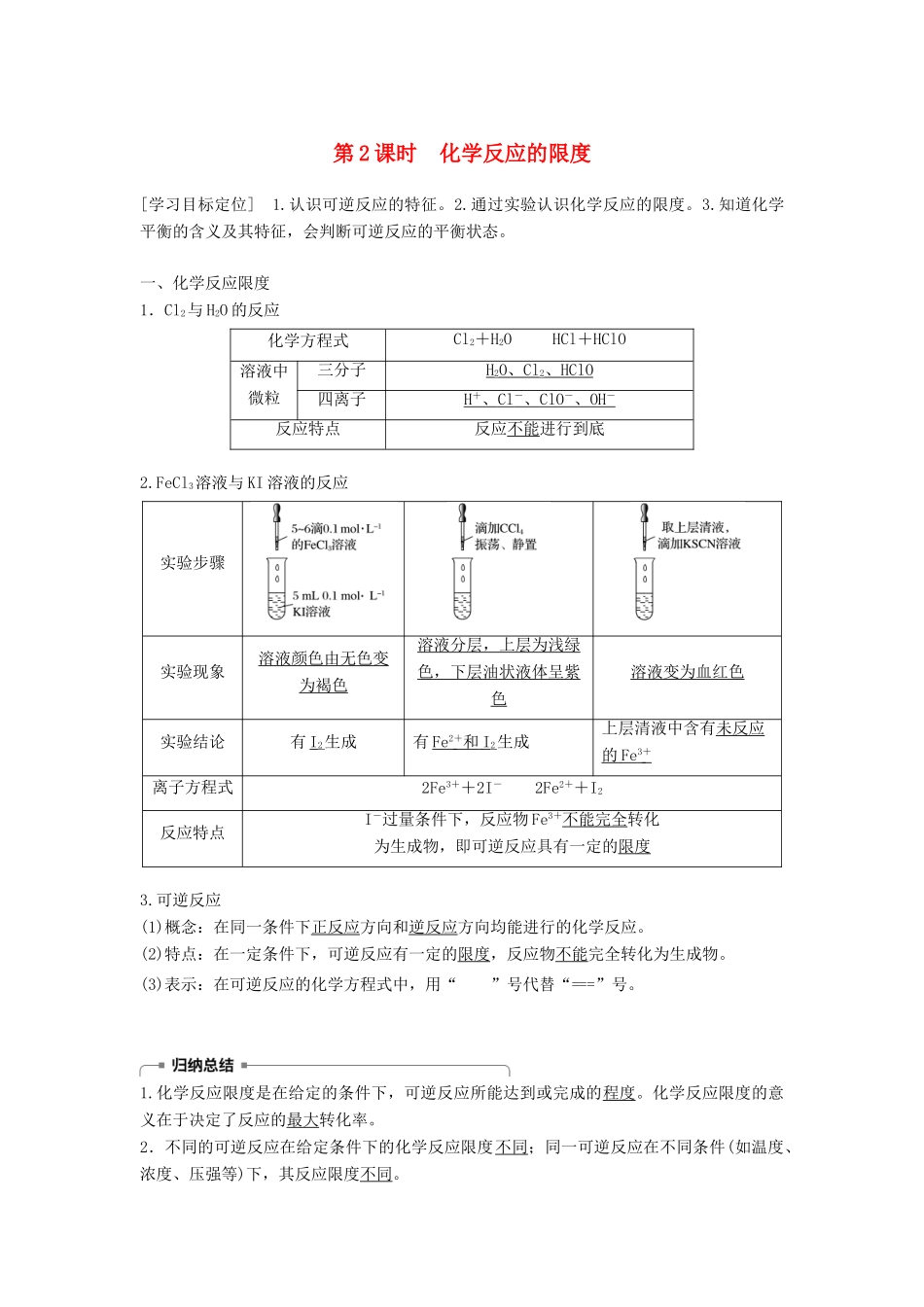
第 2 课时 化学反应的限度[学习目标定位] 1
认识可逆反应的特征
通过实验认识化学反应的限度
知道化学平衡的含义及其特征,会判断可逆反应的平衡状态
一、化学反应限度1.Cl2与 H2O 的反应化学方程式Cl2+H2O HCl+HClO溶液中微粒三分子H2O 、 Cl 2、 HClO 四离子H + 、 Cl - 、 ClO - 、 OH - 反应特点反应不能进行到底2
FeCl3溶液与 KI 溶液的反应实验步骤实验现象溶液颜色由无色变为褐色溶液分层,上层为浅绿色,下层油状液体呈紫色溶液变为血红色实验结论有 I2 生成有 Fe 2 + 和 I 2 生成上层清液中含有未反应的 Fe 3 + 离子方程式2Fe3++2I-2Fe2++I2反应特点I-过量条件下,反应物 Fe3+不能完全转化为生成物,即可逆反应具有一定的限度3
可逆反应(1)概念:在同一条件下正反应方向和逆反应方向均能进行的化学反应
(2)特点:在一定条件下,可逆反应有一定的限度,反应物不能完全转化为生成物
(3)表示:在可逆反应的化学方程式中,用“”号代替“===”号
化学反应限度是在给定的条件下,可逆反应所能达到或完成的程度
化学反应限度的意义在于决定了反应的最大转化率
2.不同的可逆反应在给定条件下的化学反应限度不同;同一可逆反应在不同条件(如温度、浓度、压强等)下,其反应限度不同
1.对于化学反应限度的叙述,错误的是( )A.任何可逆反应都有一定的限度B.化学反应达到限度时,正、逆反应速率相等C.化学反应的限度与时间的长短无关D.化学反应的限度是不可改变的答案 D解析 任何可逆反应都有一定的限度,当反应达到限度时,此时 v 正=v 逆,对同一可逆反应,当外界条件不变时,反应的限度不变,与时间长短无关,但当外界条件发生改变时,化学反应的限度也会发生改变
2.在一密闭容器中进行反应:2S