第 1 课时 化学能转化为电能[学习目标定位] 1
通过实验探究认识化学能可以转化为电能及原电池的构成条件
知道干电池、充电电池、燃料电池等发展中的化学电源的特点
会书写简单的原电池的电极反应式及电池总反应方程式(离子方程式)
一、原电池工作原理按要求完成下列实验,并填表:实验步骤①②③④现象锌片逐渐溶解,表面有气泡;铜片表面无气泡锌片逐渐溶解,铜片表面有气泡,电流计指针发生偏转两锌片逐渐溶解且表面都有气泡,电流计指针不偏转无现象解释或说明锌与稀硫酸发生置换反应产生H2,而铜则不能锌与稀硫酸反应,但氢气在铜片上产生,导线中有电流锌与稀硫酸反应产生氢气,但导线中无电流乙醇是非电解质,与 Zn 、 Cu 都 不反应根据上述实验回答下列问题:1.装置②中能量是如何转化的
具备这种特点的装置名称是什么
答案 化学能转化为电能;该装置称为原电池
2.原电池的工作原理① 分析下图并填空:原电池总反应式:Zn+2H+===Zn2++H2↑
② 能量转化过程:原电池在工作时,负极失去电子,电子通过导线流向正极,溶液中氧化性物质得到电子,发生还原反应,这样氧化反应和还原反应不断发生,闭合回路中不断有电子流产生,也就形成了电流,即化学能转变为电能
3.结合原电池工作原理及上述实验现象,分析原电池的构成条件是什么
答案 理论上,自发的氧化还原反应均可构成原电池
具体条件是① 具有活动性不同的两个电极(金属与金属或金属与能导电的非金属);② 溶液:两电极均插入电解质溶液中;③ 导线:两极用导线相连,形成闭合回路
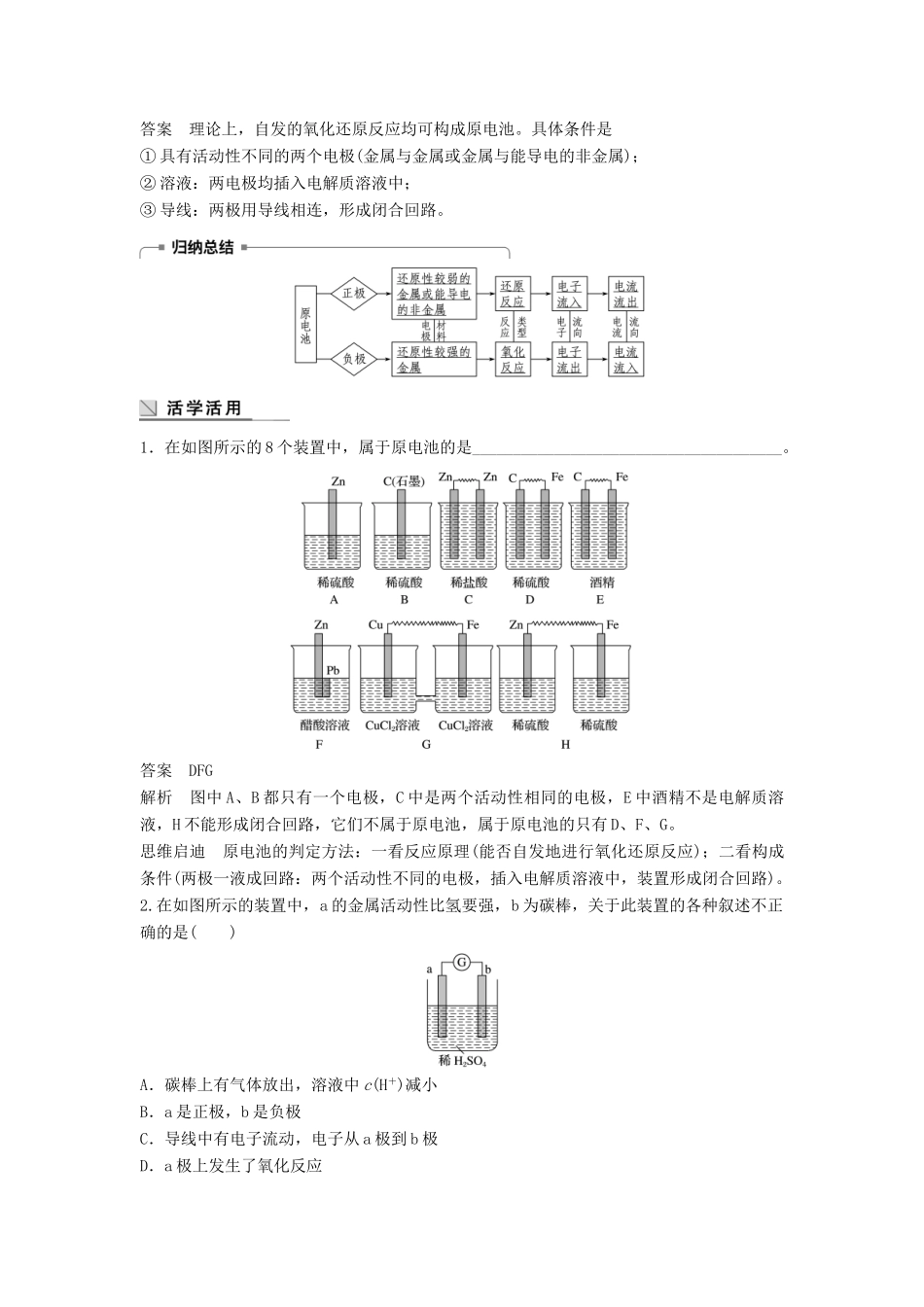
1.在如图所示的 8 个装置中,属于原电池的是______________________________________
答案 DFG解析 图中 A、B 都只有一个电极,C 中是两个活动性相同的电极,E 中酒精不是电解质溶液,H 不能形成闭合回路,它们不属于原电池,属于原电池的