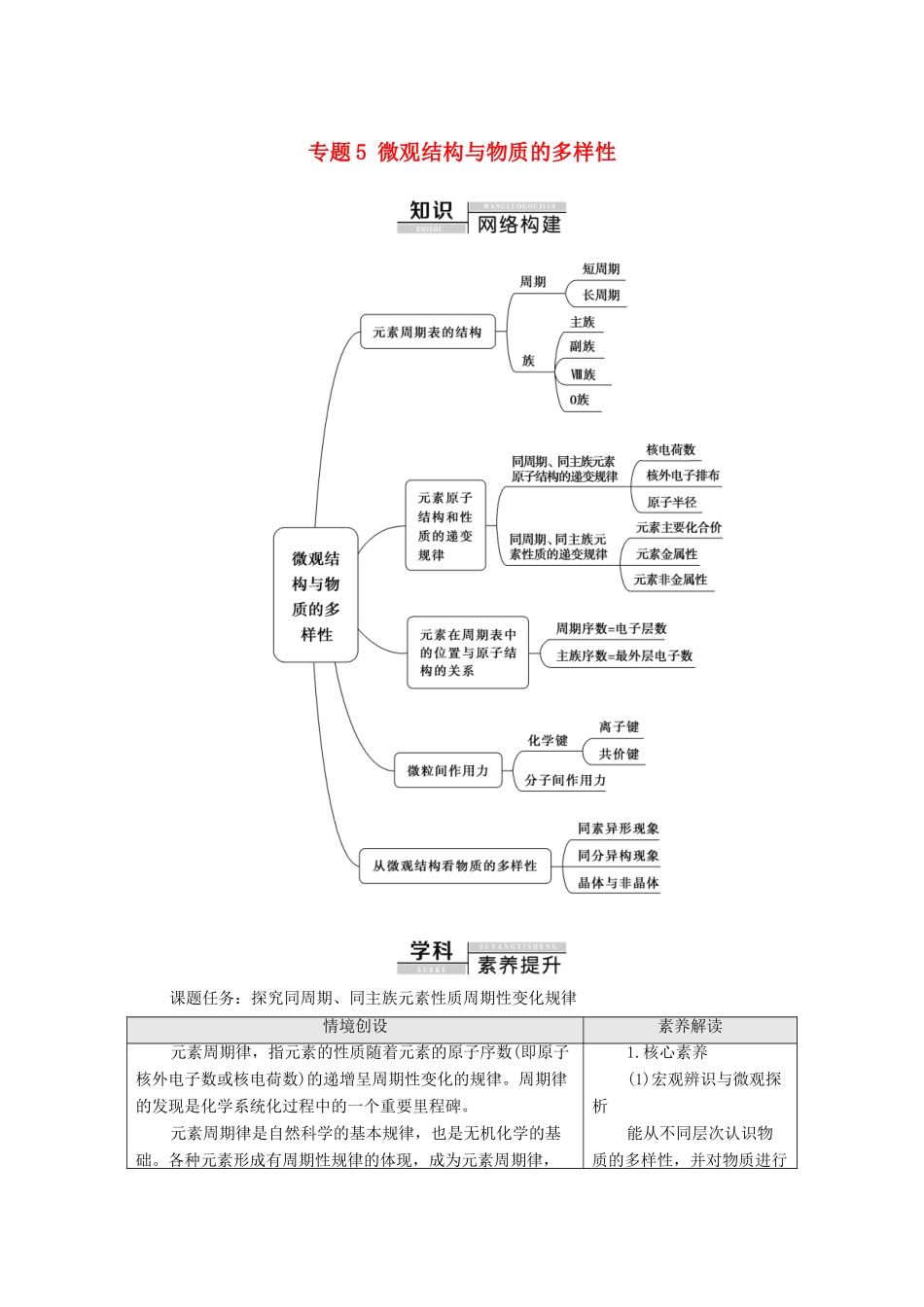
专题 5 微观结构与物质的多样性课题任务:探究同周期、同主族元素性质周期性变化规律情境创设素养解读元素周期律,指元素的性质随着元素的原子序数(即原子核外电子数或核电荷数)的递增呈周期性变化的规律。周期律的发现是化学系统化过程中的一个重要里程碑。元素周期律是自然科学的基本规律,也是无机化学的基础。各种元素形成有周期性规律的体现,成为元素周期律,1.核心素养(1)宏观辨识与微观探析能从不同层次认识物质的多样性,并对物质进行元素周期表则是元素周期律的表现形式。元素周期表是学习和研究化学的一种重要工具。元素周期表是元素周期律的具体表现形式,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。我们可以利用元素的性质、它在周期表中的位置和它的原子结构三者之间的密切关系来指导我们对化学的学习研究。了解同周期和主族元素性质的递变规律,体会元素周期律(表)在学习元素及其化合物知识及科学研究中的重要作用,是高中化学的重要任务。分类;能从元素和原子、分子水平认识物质的组成、结构、性质和变化,形成“结构决定性质”的观念。能从宏观和微观相结合的视角分析与解决实际问题。(2)认识科学探究是进行科学解释和发现、创造和应用的科学实践活动;能发现和提出有探究价值的问题;能从问题和假设出发,依据探究目的,设计探究方案,运用化学实验、调查等方法进行实验探究;勤于实践,善于合作,敢于质疑,勇于创新2.素养目标通过该探究课题的学习,认识元素周期律的基本内容,激发学生的科学探究精神,认识化学对创造物质世界的巨大贡献,增强社会责任感。探究过程素养评价【探究一】实验探究同周期、同主族元素性质递变规律某同学为了探究元素非金属性递变规律,设计了如图所示实验装置。根据强酸制弱酸的原理,所选物质要既能证明同族元素性质递变规律,又能证明同周期元素性质递变规律。所给试剂(供选择):稀盐酸、稀硝酸(易挥发)、稀硫酸、NaOH、Mg(OH)2、Al(OH)3、CaCO3、Na2SiO3溶液、Ca(ClO)2溶液。查阅资料:(1)较强酸与较弱酸的盐反应生成较弱和较强酸盐。(2)H2SiO3是一种白色胶状沉淀。(3)硝酸易挥发出 HNO3气体。请你帮他完成实验的探究过程。宏观辨识——水平 1:能从物质的类别入手,结合判断非金属性强弱的方法,确立实验目的,选择所用试剂。科学探究——水平 2:能根据实验原理设计简单实验,客观记录实验现象,并作出解释。科学探究——水平 3:能根据假设提出实验方案,独立完成...