第 1 节 原子结构模型 [课标要求]1.了解原子核外电子的运动状态
2.知道原子核外电子在一定条件下会发生跃迁,了解其简单应用
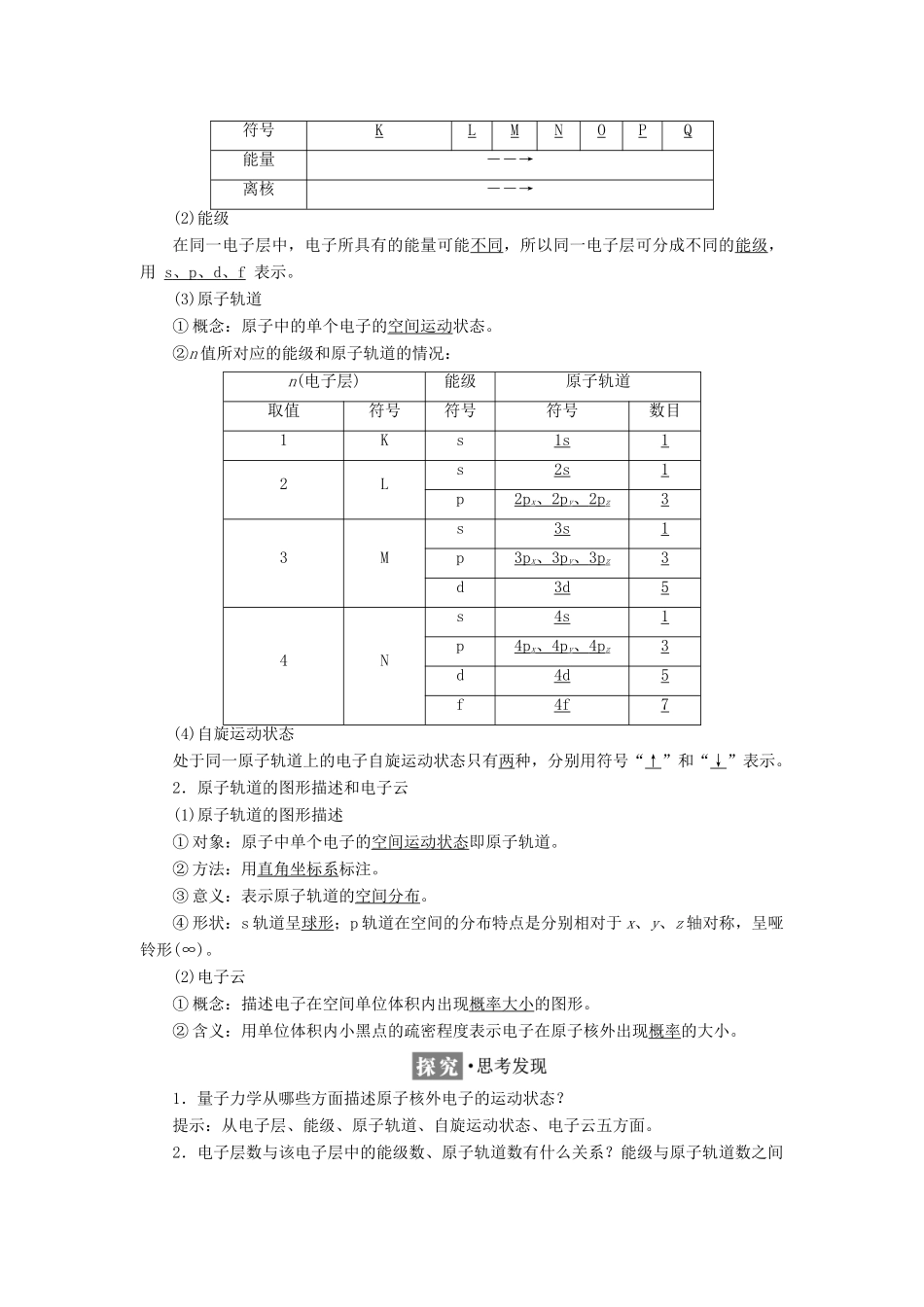
能级符号及所含轨道数:s、1,p、3,d、5,f、7
2.每个电子层所含能级类型:K:s;L:s、p;M:s、p、d;N:s、p、d、f
3.s 轨道呈球形,p 轨道呈“∞”形
4.原子轨道能量高低关系:同电子层不同能级:nf>nd>np>ns;不同电子层同能级:ns>(n-1)s>(n-2)s>(n-3)s;同电子层同能级:npx=npy=npz
1.不同时期的原子结构模型2.光谱和氢原子光谱(1)光谱① 概念:利用仪器将物质吸收的光或发射的光的波长和强度分布记录下来的谱线
② 形成原因:电子在不同轨道间跃迁时,会辐射或吸收能量
(2)氢原子光谱:属于线状光谱
3.玻尔原子结构模型的基本观点运动轨迹原子中的电子在具有确定半径的圆周轨道上绕原子核运动,并且不辐射能量能量分布在不同轨道上运动的电子具有不同的能量,而且能量是量子化的
轨道能量依 n(电子层数)值(1,2,3,…)的增大而升高电子对氢原子而言,电子处于 n=1 的轨道时能量最低,称为基态;能量高于基态的状态跃迁称为激发态
电子在能量不同的轨道之间跃迁时,辐射或吸收的能量以光的形式表现出来并被记录下来,就形成了光谱[特别提醒] (1)基态原子激发态原子
(2)基态原子和激发态原子的相互转化时吸收或释放能量,形成光谱
(3)焰色反应产生的原因是原子中的电子在能量不同轨道上跃迁
1.判断正误(正确的打“√”,错误的打“×”)
(1)门捷列夫提出原子学说,并发现元素周期律
( )(2)氢原子外围只有一个电子,故氢原子光谱只有一条谱线
( )(3)氢原子光谱属于线状光谱
( )(4)基态氢原子转变成激发态氢原子时释放能量
( )(5)焰色反应与电子跃迁有关,属于化学变化