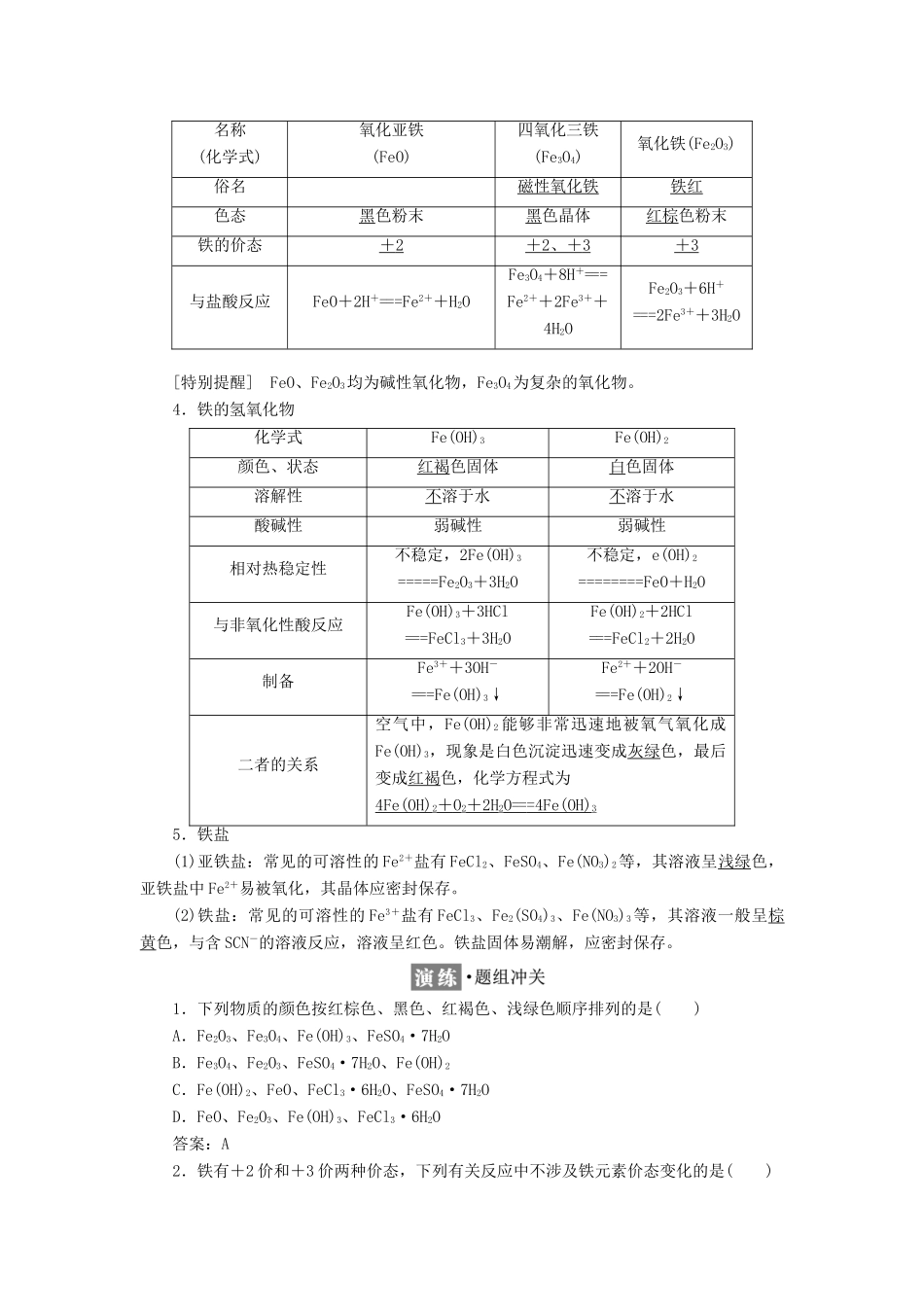
第 3 课时 探究铁及其化合物的氧化性或还原性—————————————————————————————————————[课标要求]1.了解铁及其化合物的主要化学性质,理解其氧化性、还原性的特点。2.了解 Fe、Fe2+、Fe3+之间的相互转化。3.掌握 Fe2+、Fe3+的检验方法。4.了解铁与人体健康的关系,认识化学知识与人类生活的密切联系。,1.地壳中含量排前四位的元素依次为:O、Si、Al、Fe。2.铁元素常见的三种化合价:0 价、+2 价、+3 价。3.Fe3+的检验方法:向待检液中滴入 KSCN 溶液,溶液呈红色,说明溶液中含有 Fe3+。4.Fe2+的检验方法:向待检液中滴入 KSCN 溶液,无明显现象,再滴入新制氯水溶液变红色,说明溶液中含有 Fe2+。5.Fe(OH)2 在空气中变质现象:白色→灰绿色→红褐色,反应为 4Fe(OH)2+O2+2H2O===4Fe(OH)3。6.重要的离子方程式:2Fe3++Fe===3Fe2+2Fe2++Cl2===2Fe3++2Cl-Cu+2Fe3+===2Fe2++Cu2+1.铁元素的存在(1)含量铁元素在地壳中含量仅次于氧、硅、铝三种元素。(2)存在形态① 游离态:存在于陨铁中。② 化合态:主要以+ 2 、+ 3 价铁的化合物存在。2.铁单质(1)物理性质光亮的银白色金属,有良好的延展性,易导电导热,能被磁铁吸引。有较高的硬度、密度和熔、沸点,纯铁有很强的抗腐蚀力。(2)化学性质(写出化学方程式或离子方程式)3.铁的氧化物名称(化学式)氧化亚铁(FeO)四氧化三铁(Fe3O4)氧化铁(Fe2O3)俗名磁性氧化铁铁红色态黑色粉末黑色晶体红棕色粉末铁的价态+ 2 + 2 、+ 3 + 3 与盐酸反应FeO+2H+===Fe2++H2OFe3O4+8H+=== Fe2++2Fe3++4H2OFe2O3+6H+===2Fe3++3H2O[特别提醒] FeO、Fe2O3均为碱性氧化物,Fe3O4为复杂的氧化物。4.铁的氢氧化物化学式Fe(OH)3Fe(OH)2颜色、状态红褐色固体白色固体溶解性不溶于水不溶于水酸碱性弱碱性弱碱性相对热稳定性不稳定,2Fe(OH)3=====Fe2O3+3H2O不稳定,e(OH)2========FeO+H2O与非氧化性酸反应Fe(OH)3+3HCl===FeCl3+3H2OFe(OH)2+2HCl===FeCl2+2H2O制备Fe3++3OH-===Fe(OH)3↓Fe2++2OH-===Fe(OH)2↓二者的关系空气中,Fe(OH)2 能够非常迅速地被氧气氧化成Fe(OH)3,现象是白色沉淀迅速变成灰绿色,最后变成红褐色,化学方程式为4Fe(OH)2+ O 2+ 2H 2O == =4Fe(OH) 35.铁盐(1)亚铁盐:常见的可溶性的 Fe2+盐有 FeCl2、FeSO4、Fe(NO3)2等,其溶液呈浅绿色,亚铁盐中 ...