第一节 化学能与热能学习目标核心素养1
理解化学反应中能量变化的主要原因—化学键的断裂和形成
2.了解吸热反应和放热反应的概念,熟知常见的吸热反应和放热反应
宏观辨识:理解化学反应中能量的变化取决于反应物与生成物的总能量相对大小
2.微观探析:从化学键的断裂和形成,在本质上认识化学能量与化学变化的本质
一、化学反应中的能量变化1.化学反应中能量变化的原因——微观角度(1)化学反应的实质原子之间重新组合,是反应物中旧化学键断裂和生成物中新化学键形成的过程
(2)化学反应中能量变化的原因① 变化原因② 实例a.断裂 1 mol H—H 键(H—H→2H)吸收 436 kJ 能量,形成 1 mol H—H 键(2H→H—H)放出 436 kJ 能量;b.断裂 4 mol C—H 键(CH4→C+4H)吸收 1660 kJ 能量,形成 1 mol C—H 键(C+H→C—H)放出 415 kJ 能量
③ 结论化学反应中能量变化的主要原因是化学键的断裂与形成
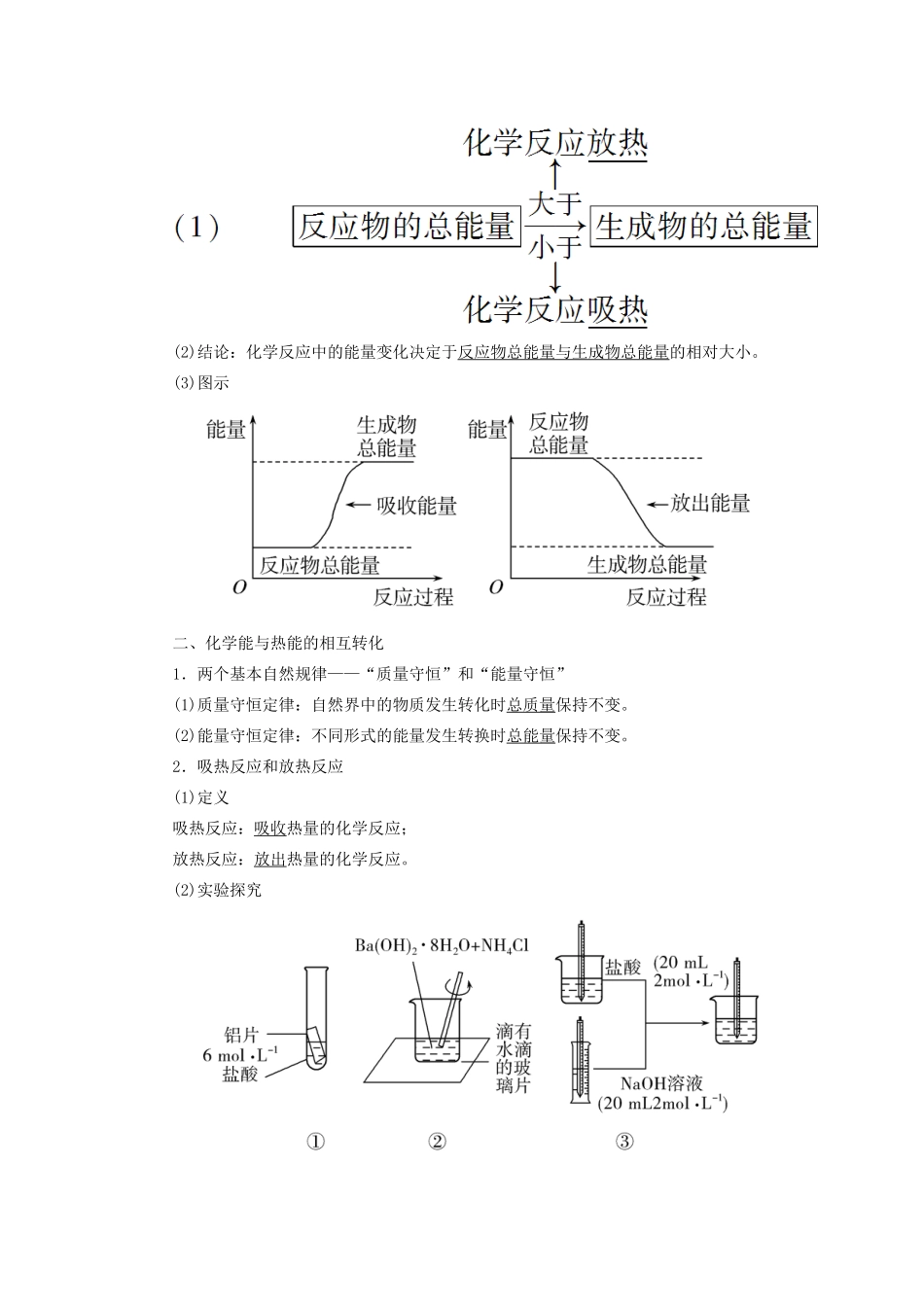
2.化学反应中能量变化的决定因素——宏观角度(2)结论:化学反应中的能量变化决定于反应物总能量与生成物总能量的相对大小
(3)图示二、化学能与热能的相互转化1.两个基本自然规律——“质量守恒”和“能量守恒”(1)质量守恒定律:自然界中的物质发生转化时总质量保持不变
(2)能量守恒定律:不同形式的能量发生转换时总能量保持不变
2.吸热反应和放热反应(1)定义吸热反应:吸收热量的化学反应;放热反应:放出热量的化学反应
(2)实验探究① 铝和稀盐酸的反应②Ba(OH)2·8H2O 和氯化铵反应③ 盐酸与氢氧化钠反应三、人类对能源的利用1.化学能与热能转化的应用(1)化学能通过化学反应转化成热能,为人类的生存和发展提供了所需要的能量和动力,如化石燃料的燃烧、炸药开山、发射火箭等
(2)热能转化为化学能是人们进行化学科学研究、研制新物