第二章《化学反应的方向、限度和速率》复习教学案[教学目标]1.知识目标巩固本章知识
2.能力和方法目标提高综合分析能力和知识的综合运用能力
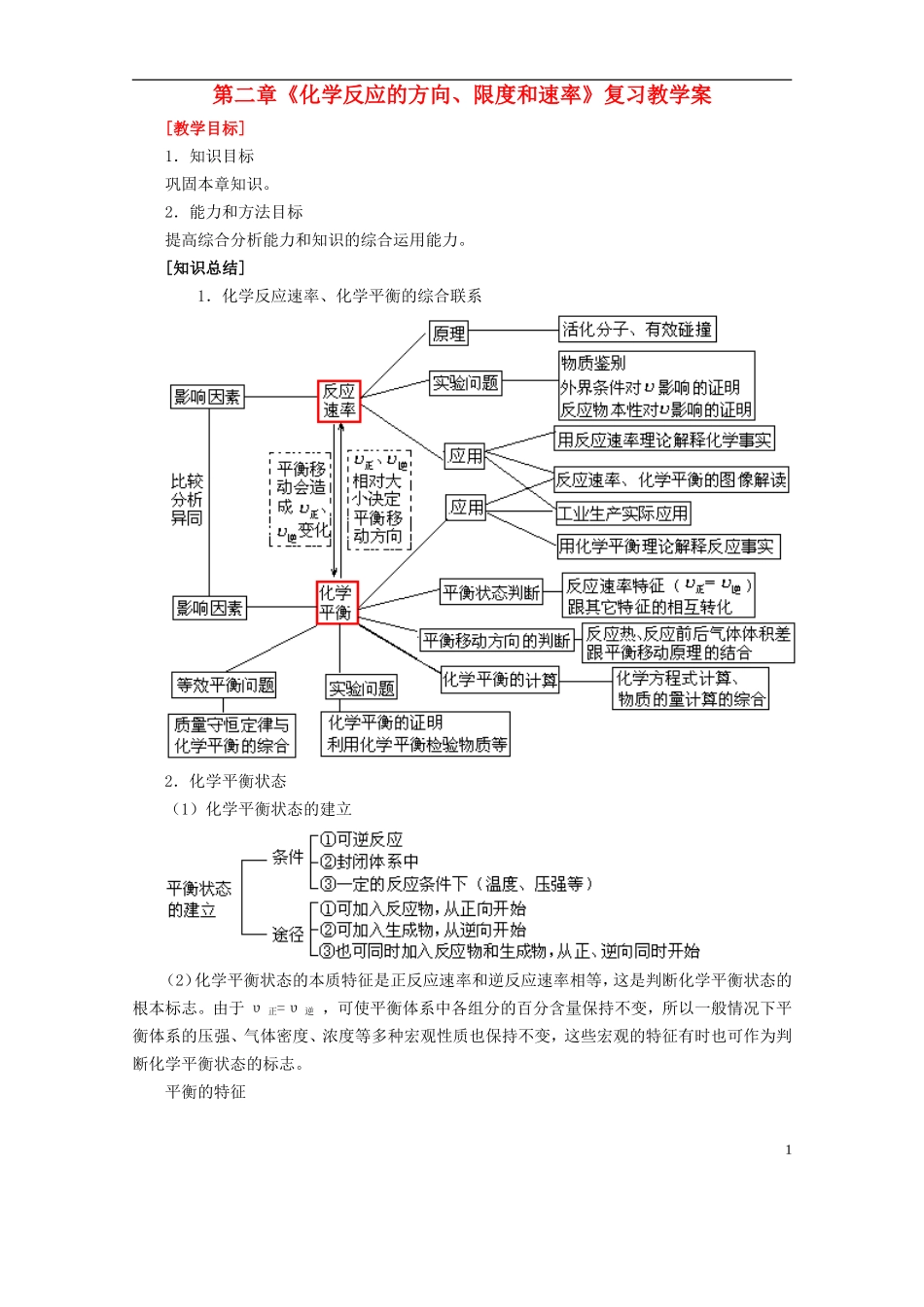
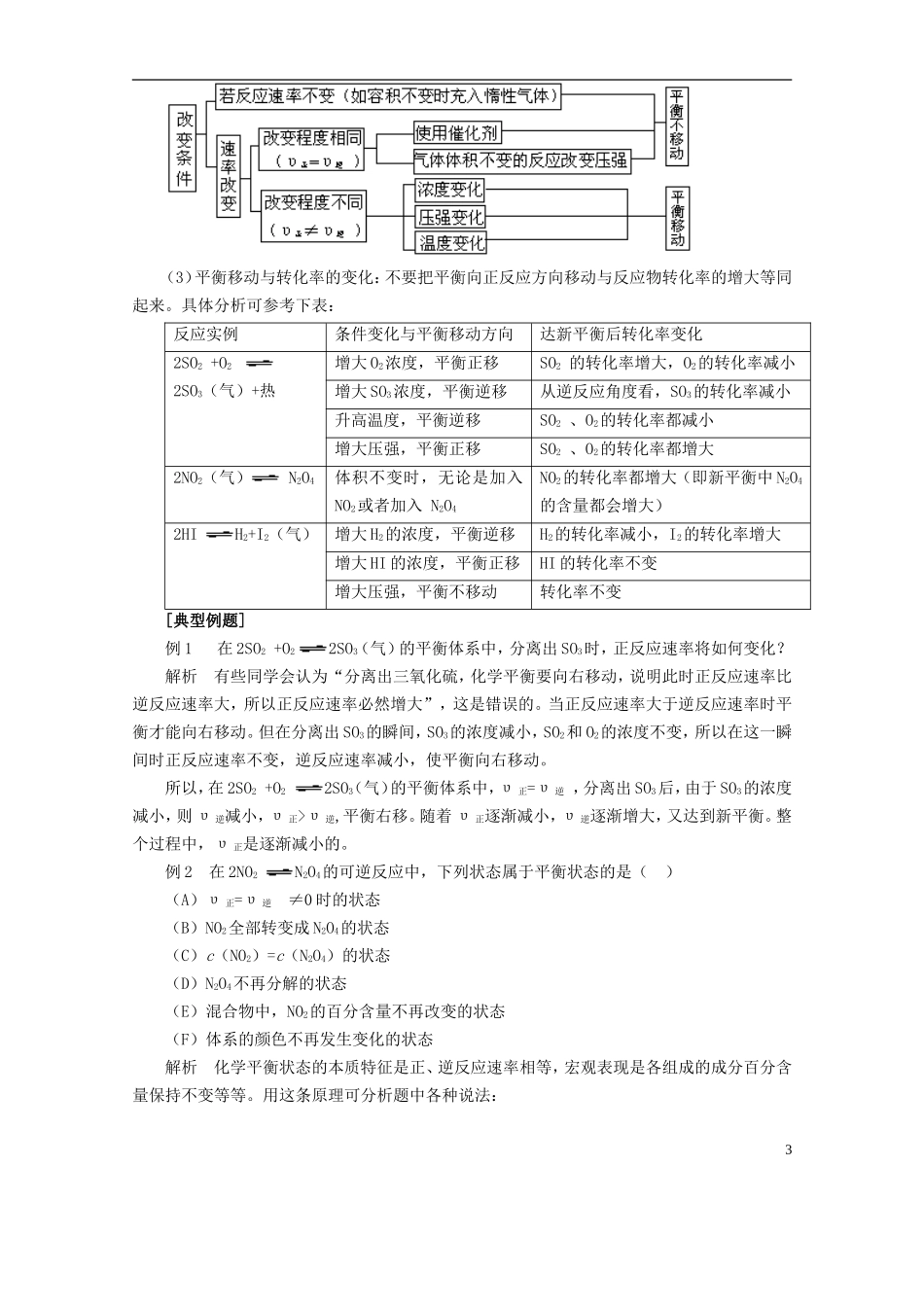
[知识总结] 1.化学反应速率、化学平衡的综合联系2.化学平衡状态(1)化学平衡状态的建立(2)化学平衡状态的本质特征是正反应速率和逆反应速率相等,这是判断化学平衡状态的根本标志
由于 υ 正=υ 逆 ,可使平衡体系中各组分的百分含量保持不变,所以一般情况下平衡体系的压强、气体密度、浓度等多种宏观性质也保持不变,这些宏观的特征有时也可作为判断化学平衡状态的标志
平衡的特征1五大特点化学平衡逆可逆反应 等υ(正)=υ(逆)≠0动动态平衡定各组分含量一定,体积一定时,浓度就一定;有平衡转化率变浓度、温度、压强改变化学平衡即发生移动定量特征一定温度下,化学平衡常数保持不变(3)化学平衡状态的判断举例反应mA(g)+nB(g) pC(g)+qD(g)混合物体系中各成分的含量① 各物质的物质的量或各物质的物质的量分数一定平衡② 各物质的质量或各物质的质量分数一定平衡③ 各气体的体积或体积分数一定平衡④ 总压强、总体积、总物质的量一定不一定平衡正、逆反应速率的关系① 在单位时间内消耗了 m molA 同时生成 m molA,即 v 正=v 逆平衡② 在单位时间内消耗了 n molB 同时生成 p molC,则 v 正=v 逆平衡③vA:vB:vC:vD=m:n:p:q,v 正不一定等于 v 逆不一定平衡④ 在单位时间内生成了 n molB,同时消耗 q molD,因均指 v 逆不一定平衡压强①m+n≠p+q 时,总压力一定(其他条件一定)平衡②m+n=p+q 时,总压力一定(其他条件一定)不一定平衡混合气体的平均分子量()①一定时,只有当 m+n≠p+q 时,平衡②一定,但 m+n=p+q 时不一定平衡温度任何化学反应都伴随着能量变化,在其他条件不