第十七章 铜、锌分族Chapter 17 The Copper Subgroup and Zinc Subgroup 从本章开始,我们要讲 ds 区、d 区和 f 区元素的性质
铜(copper, cuprum)、银(silver, argentum)和金(gold, aurum)位于长周期表中 IB 族,通常称为铜族元素,又称货币金属(coinage metal)
锌(zinc)、镉(cadmium)和汞(mercury, hydrargyrum)位于长周期 IIB 族,通常称为锌分族
§17-1 铜分族The Copper Subgroup一、General Properties 1.The first ioniz ation energy (I1) Cu:7
726eV Ag:7
576eV Au:9
226eV IB 族元素的第一电离能比 IA 族元素的第一电离能高得多,这是因为 ns电子穿透了(n1)d10电子的屏蔽;从 Cu 到 Ag 第一电离能降低是因为 Ag 有较高的主量子数,价电子离核远,较易失去价电子,而 Au 的第一电离能却更大,这是由于Au 的 6s 电子不仅穿透 5d 而且还穿透 4f 电子的屏蔽
2.Oxidation state:呈+1、+2、+3 氧化态各元素的特征氧化态为: +2 +1 +3 其中 Ag 的+1 氧化态之所以稳定,是因为 4d1 0电子构型相对较高的稳定性,例如 Pd 的电子排布为 4d105s0,是一个很好的说明
3.Covalent properties: Cu、Ag、Au 形成共价键的倾向大于碱金属形成共价键的倾向
例如Cu2、Ag2、Au2的离解能分别为 174、158 和 210kJ·mol1,这是由于它们两个原子之间的空的 np 轨道与(n1)d 轨道上的电子对形成的附加 π 键所致
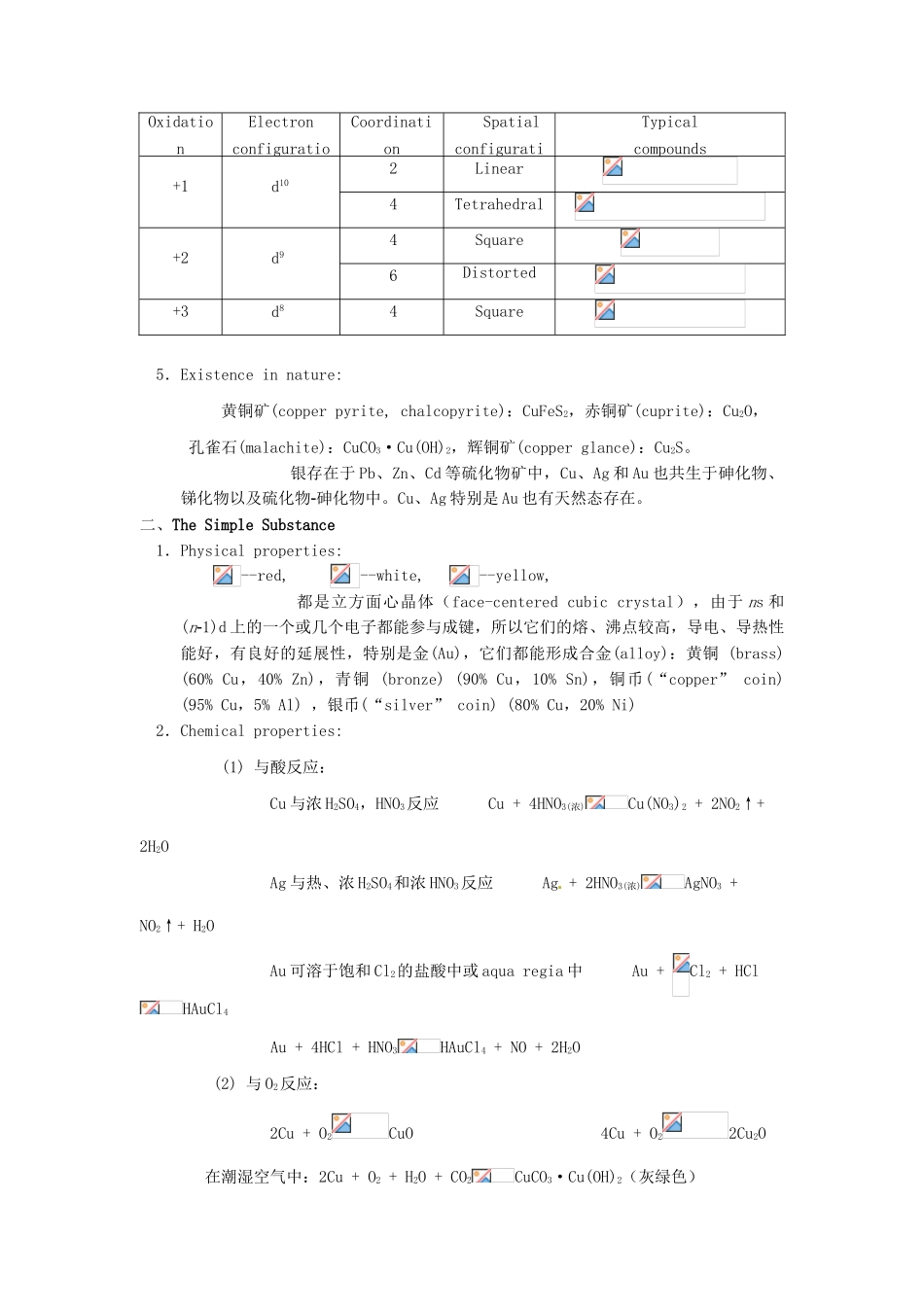
4.Comp