中学有机“官能团”的复习摘要:本文总结了常见官能团的性质、引入及检验,以供复习参考
关键词:官能团 化学性质官能团是决定有机物特殊化学性质的原子或原子团,中学阶段常见的官能团有碳碳双键、碳碳叁键、羟基、羧基、醛基、酯基,下面对这些常见的官能团进行简单归纳,以供学习和复习参考
一、官能团的基础知识—C C——C C—化学性质氧化反应:使酸性 KMnO4溶液褪色加成反应:与 H2 、 X2 、 HX 、 H2O 等反应加聚反应检验使溴水褪色使酸性 KMnO4溶液褪色引入:醇和卤代烃的消去1、卤原子—X化学性质水解:NaOHR—X + H2O R—OH + HX ( 反应条件:强碱的水溶液 )消去:—C—C— + NaOH —C=C— + NaX + H2O 醇△HX ( 消去反应条件:强碱的醇溶液 )卤原子的检验:试样 NaOH△HNO3酸化AgNO3 据沉淀颜色确定 X卤原子的引入:主要通过计算关系: R—X ~ AgX3、加成反应取代反应:卤代、硝化、磺化加成反应:催化剂△+3H2苯的同系物(与苯环相连的碳有 H )能使酸性高锰酸钾溶液褪色2、( 一 般 不 考虑 为 官 能团)醇羟基—OH化学性质与活泼金属反应: 2ROH + 2Na → 2RONa + H2↑消去反应:H—C—C— —C=C— + H2O 浓硫酸△ (或 170℃ )OH催化氧化:2—C—O H + O2 2 +2H2OCu 或 Ag △—C— OH酯化反应分 子 间 脱 水 成醚:ROH + R'OHR—O—R' + H2O浓硫酸△引入:卤代烃的水解、烯烃与水反应、醛基的加氢还原计算关系: 2—OH ~ H24、(邻碳去氢)(同碳去氢) 注意区别:中学化学中常涉及到三种羟基:醇羟基、酚羟基和羧羟基
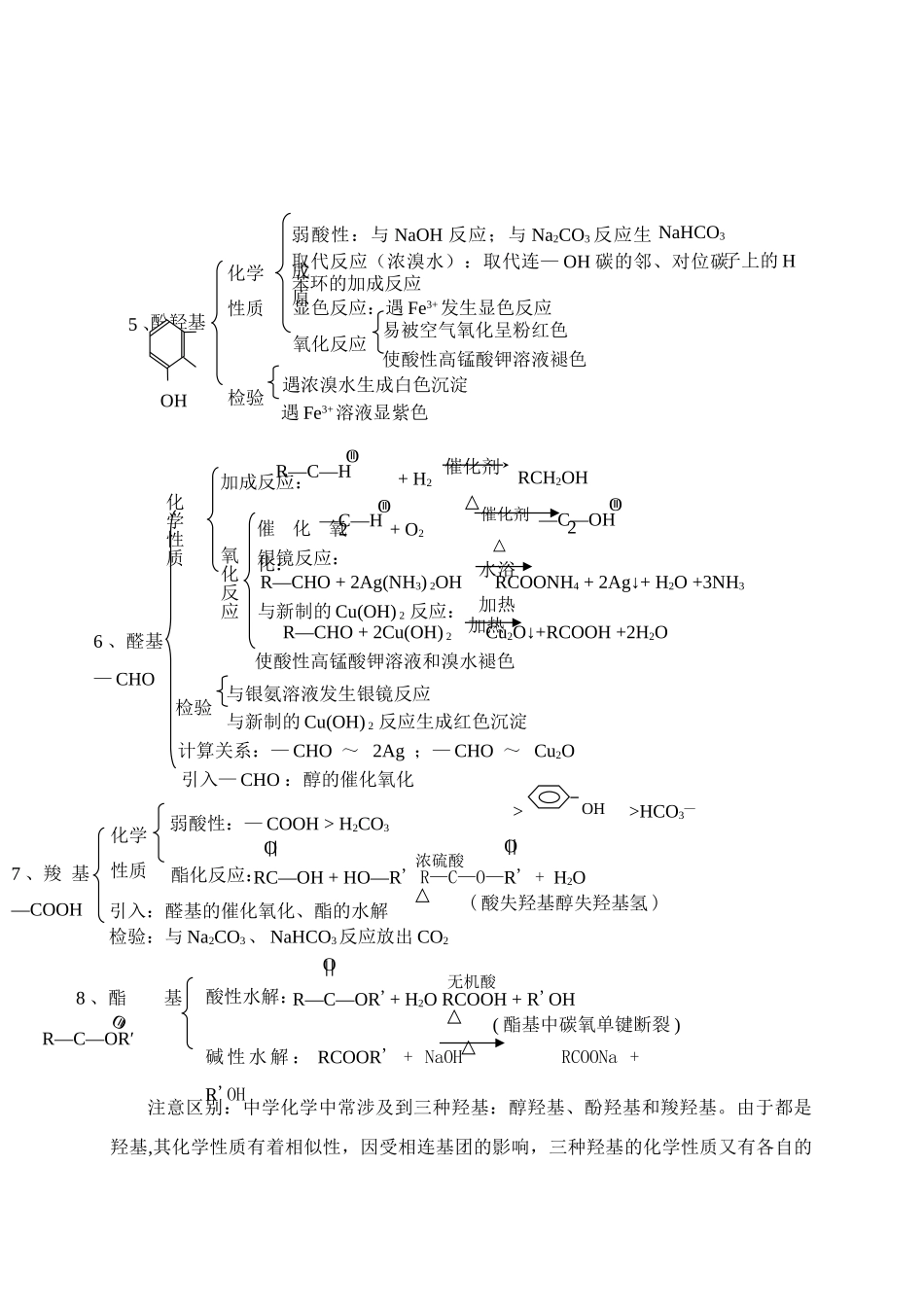
由于都是羟基,其化学性质有着相似性,因受相连基团的影响,三种羟基的化学性质又有各自的