牛乳中酪蛋白得制备与浓度测定一、实验目得1、学习从牛乳中分离酪蛋白得原理与方法2、掌握等电点沉淀法提取蛋白质得方法3、了解紫外吸收法测定蛋白质浓度得原理,熟悉紫外分光光度计得使用4、学会用考马斯亮蓝结合法测定蛋白质浓度二、实验原理1、准备酪蛋白原理:牛乳中主要含有酪蛋白与乳清蛋白两种蛋白质,其中酪蛋白占了牛乳蛋白质得 80%、牛乳在 PH 4
7 时酪蛋白等电聚沉后剩余得蛋白质统称为乳清蛋白、酪蛋白就是白色、无味得物质,不溶于水、乙醇等有机溶剂,但溶于碱溶液
乳清蛋白不同于酪蛋白,其粒子得水与能力很强,分散性高,在乳中呈高分子状态
本法利用等电点时溶解度最低得原理,将牛乳得 PH 调至 4
7时,酪蛋白就沉淀出来
用乙醇洗涤沉淀物,除去脂类杂质后便可得到纯得酪蛋白
2、紫外吸收法测定蛋白质浓度得原理:大多数蛋白质由于有酷氨酸与色氨酸得存在,在紫外光 280nm 有吸收高峰,可以进行蛋白质含量得测定
但就是核酸在2 80nm 也有吸收,干扰测定,不过核酸得最大吸收峰在26 0nm,通过测定在28 0 nm 与 260 nm时A得比值,然后通过计算消除核酸存在得影响,可以求得有核酸存在时蛋白质得浓度
3、考马斯亮蓝结合法测定蛋白质浓度原理:考马斯亮蓝能与蛋白质得疏水微区相结合,这种结合具有高敏感性
考马斯亮蓝G 250 得磷酸溶液呈棕红色,最大吸收峰在 465nm、当它与蛋白质结合形成复合物时呈蓝色,其最大吸收峰改变为 5 9 5n m,考马斯亮蓝 G 2 5 0—蛋白质复合物得高消光效应导致了蛋白质定量测定得高敏感度
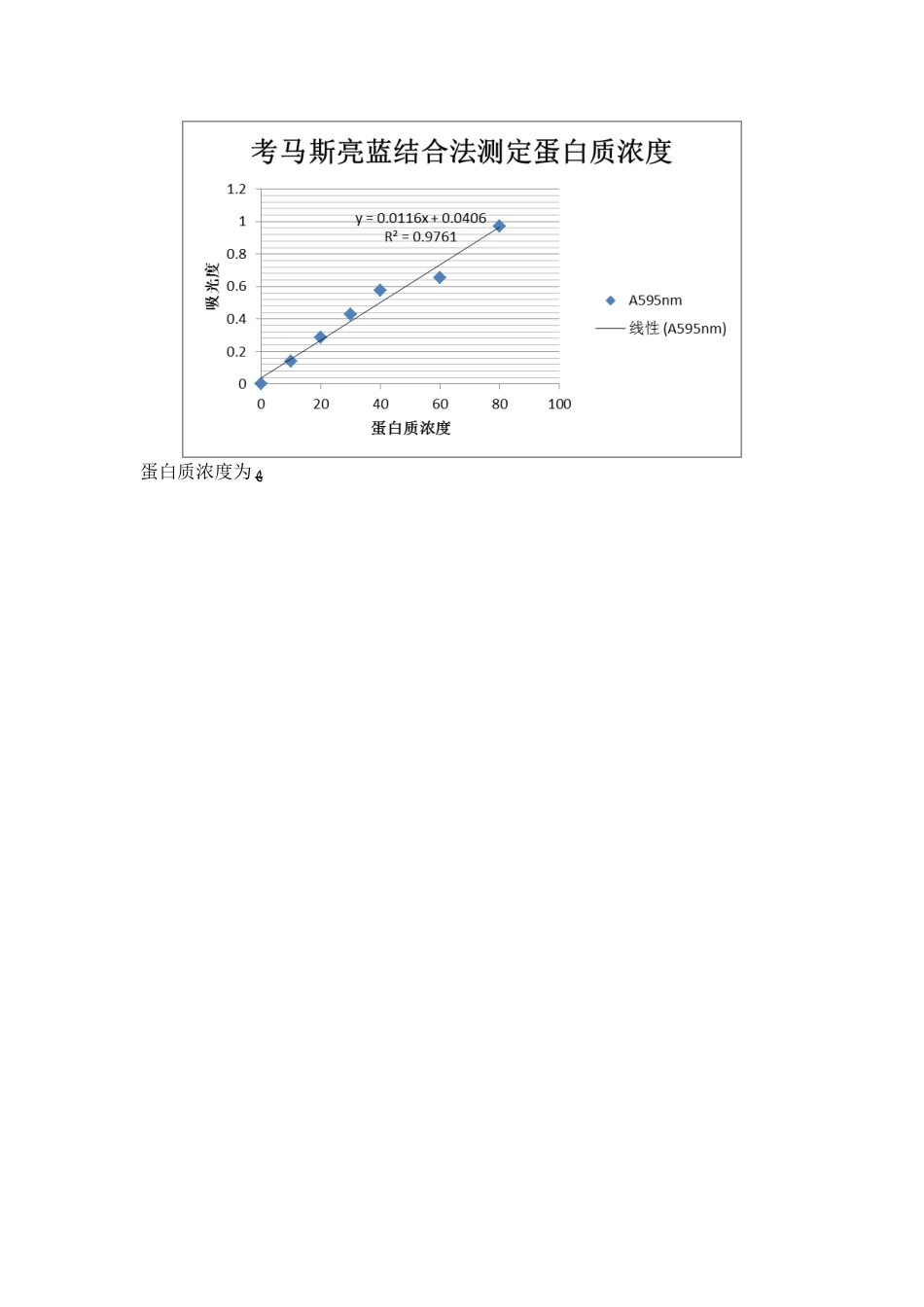
在一定范围内,考马斯亮蓝 G250—蛋白质复合物呈色后,在 595nm 下,吸光度与蛋白质含量呈线性关系,故可以用于蛋白质浓度得测定
三、实验器材与试剂1、制备酪蛋白:烧杯、玻璃棒、量筒、精密 PH 试纸、离心机、布氏漏斗、表面皿、恒温水浴锅牛奶、醋酸缓冲液、冰