第 12 讲 大自然中的二氧化碳 考点一 二氧化碳的制取 1.反应原理 利用大理石或石灰石和稀盐酸反应制取,反应的化 学 方 程 式 为 CaCO3 + 2HCl===CaCl2 + H2O +CO2↑
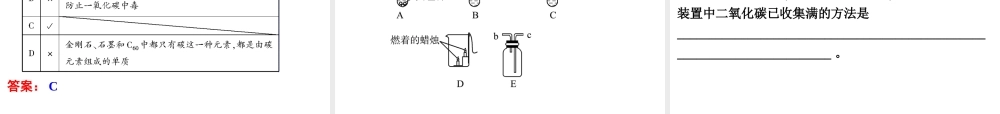
2.实验装置 3.收集和验满方法 收集方法:向上排空气法
验满:将燃烧的木条放在集气瓶口,木条熄灭说明已收集满
4.检验方法 将澄清石灰水倒入集气瓶中振荡,溶液变浑浊,说明气体为 CO2
5.干燥方法 通常使用浓硫酸对 CO2 进行干燥,不能使用碱石灰、烧碱固体进行干燥
考点二 二氧化碳的性质及用途 1.二氧化碳的性质 (1)物理性质 通常状况下,CO2 是无色、无味的气体,密度比空气大,能溶于水
固体 CO2 俗称干冰,可作制冷剂
(2)化学性质 ①既不燃烧,也不支持燃烧 如图Ⅰ,向放有阶梯蜡烛的烧杯中倾倒 CO2,观察到下面的蜡烛先熄灭上面的蜡烛后熄灭,这个实验说明:a
CO2 的密度比空气大;b
CO2 既不燃烧也不支持燃烧,故 CO2 可用于灭火
②与水反应 如图Ⅱ,CO2 通入紫色石蕊试液中生成碳酸(或H2CO3)使试液由紫色变为红色,反应的化学方程式为H2O+CO2===H2CO3,碳酸不稳定,易分解,反应的化学方程式为 H2CO3===H2O+CO2↑
③与碱反应 如图Ⅲ,向澄清石灰水中通入 CO2,澄清石灰水变浑浊,这是由于生成了白色不溶物碳酸钙的缘故,其化学方程式为 CO2+Ca(OH)2===CaCO3↓+H2O,这个反应可用来检验 CO2 气体
④不能供给呼吸 二氧化碳本身没有毒性,但当空气中的 CO2 超过正常含量时,会对人体健康产生影响
在进入久未开启的菜窖、干涸的深井和深洞底部之前,必须先做灯火试验
2.用途 (1)用于灭火 (2)作气体肥料 (3)作化工产品的原料(生产尿素、汽水、制纯碱) (4)干冰作制冷剂 考点三 温室效