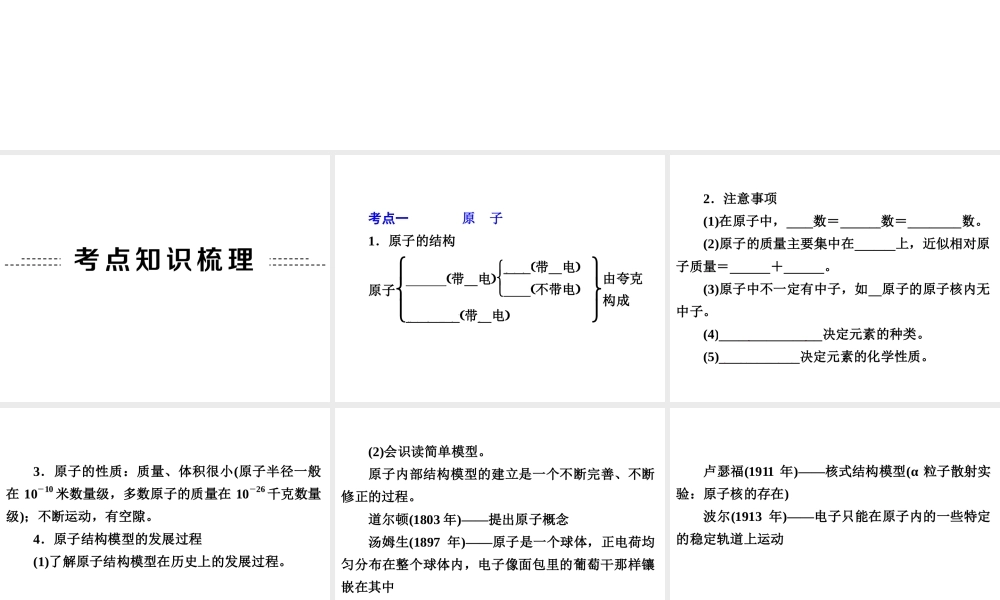
专题 26 物质的构成和组成 考点一 原 子 1.原子的结构 原子原子核带正电 质子带正电中子不带电核外电子带负电由夸克构成 2.注意事项 (1)在原子中,质子数=核电荷数=核外电子数
(2)原子的质量主要集中在原子核上,近似相对原子质量=质子数+中子数
(3)原子中不一定有中子,如氢原子的原子核内无中子
(4)质子(或核电荷)数决定元素的种类
(5)最外层电子数决定元素的化学性质
3.原子的性质:质量、体积很小(原子半径一般在 10-10 米数量级,多数原子的质量在 10-26 千克数量级);不断运动,有空隙
4.原子结构模型的发展过程 (1)了解原子结构模型在历史上的发展过程
(2)会识读简单模型
原子内部结构模型的建立是一个不断完善、不断修正的过程
道尔顿(1803 年)——提出原子概念 汤姆生(1897 年)——原子是一个球体,正电荷均匀分布在整个球体内,电子像面包里的葡萄干那样镶嵌在其中 卢瑟福(1911 年)——核式结构模型(α 粒子散射实验:原子核的存在) 波尔(1913 年)——电子只能在原子内的一些特定的稳定轨道上运动 考点二 分子与离子 1.分子 分子是保持物质化学性质的最小粒子
2.离子是带电的原子或原子团
3.分子、原子、离子间的区别与联系 考点三 元 素 1.元素是指具有相同核电荷数(即质子数)的一类原子的总称
2.分布 (1)地壳中含量居前 5 位的元素分别为 O、Si、Al、Fe、Ca
(2)人体中含量居前 4 位的元素分别是 O、C、H、N
(3)海水中除了水由 H、O 两种元素组成外,含量较高的元素是 Na 和 Cl,即海水中含量最高的盐是NaCl
3.化肥中的重要元素 植物生长需要多种元素,农业上常用的化肥是氮肥、磷肥、钾肥
元素 原子 定义 具有相同核电荷数的一类原子的总