课题一 质量守恒定律 分子-→原子--→新分子--→新物质分成 重新组合 聚集成想一想:水通电分解是什么变化
一、提出问题:化学变化中各物质的质量是否发生改变呢
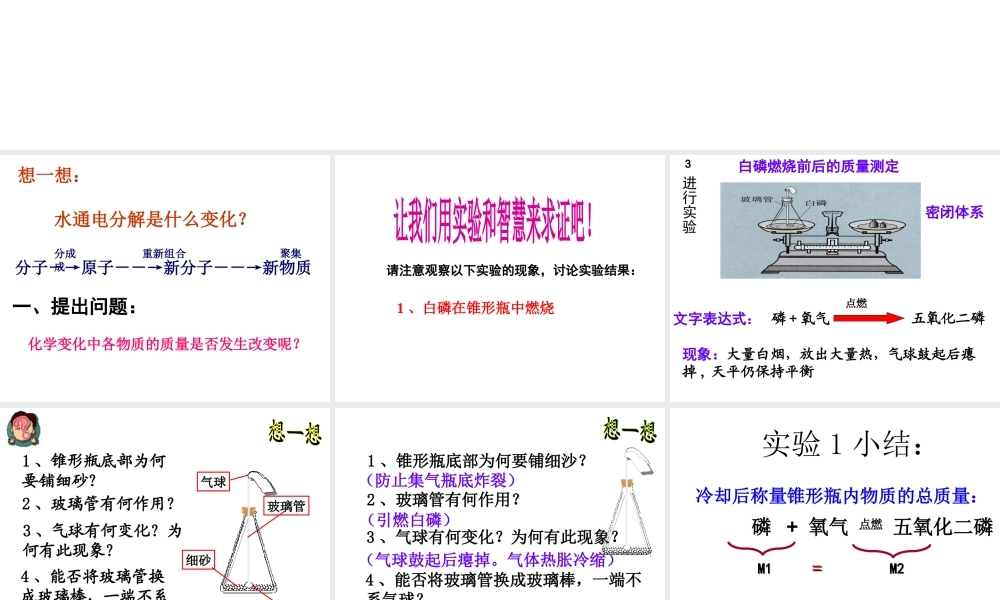
请注意观察以下实验的现象,讨论实验结果:1 、白磷在锥形瓶中燃烧现象:大量白烟,放出大量热,气球鼓起后瘪掉 , 天平仍保持平衡文字表达式: 磷 + 氧气点燃五氧化二磷白磷燃烧前后的质量测定进行实验3密闭体系1 、锥形瓶底部为何要铺细砂
2 、玻璃管有何作用
3 、气球有何变化
为何有此现象
4 、能否将玻璃管换成玻璃棒,一端不系气球
细砂玻璃管气球白磷(防止集气瓶底炸裂)(引燃白磷)(气球鼓起后瘪掉
气体热胀冷缩)(不能,由于气压过大,瓶塞易被冲出)1 、锥形瓶底部为何要铺细沙
2 、玻璃管有何作用
3 、气球有何变化
为何有此现象
4 、能否将玻璃管换成玻璃棒,一端不系气球
实验 1 小结: 磷 + 氧气 点燃 五氧化二磷 M1 M1 M2M2冷却后称量锥形瓶内物质的总质量:== 2 、铁与硫酸铜溶液反应请注意观察以下实验现象,讨论实验结果:实验 2 小结: 铁 + 硫酸铜→铜 + 硫酸亚铁 M1 M2将铁钉浸到硫酸铜溶液中,观察到的现象:铁钉表面变成红色,溶液颜色由蓝色变成浅绿色称量烧杯中物质的总质量:=通过实验我们能得到什么结论
通过实验我们能得到什么结论
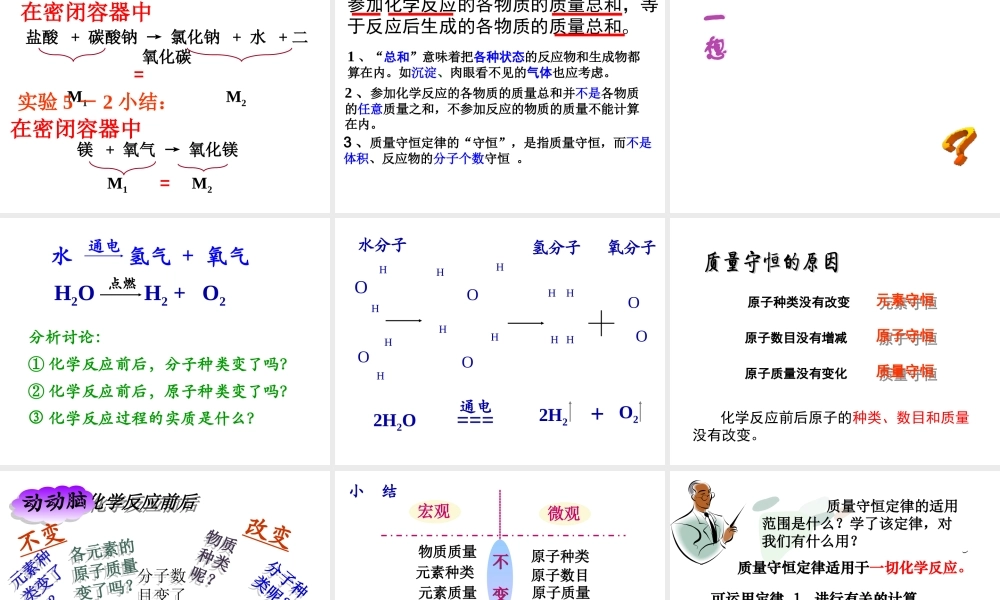
无数实验证明:无数实验证明: 参加化学反应的各物质的质量 参加化学反应的各物质的质量总和,等于反应后生成的各物质的总和,等于反应后生成的各物质的质量总和
这个规律叫做质量守恒质量总和
这个规律叫做质量守恒定律
反应物反应物生成物生成物实验 5 - 1 : 实验 5 - 2 :镁 + 氧气氧化镁点燃完全燃烧后称量留下固体的质量比反应前镁带的质量不相等
如何解释如何解释 在实验中,稀盐酸和碳酸钠反应前后物质的总质量为什么不相等呢
现象:固体消失,产生大